Закон на историята на Бойл-Мариот, математически израз, примери
Законът на Бойл е това, което изразява връзката между налягането, упражнявано от или върху газ, и обема, зает от него; поддържане на постоянна температура на газа, както и неговото количество (брой молове).
Този закон, заедно с този на Чарлз, Гей-Люсак, Чарлз и Авогадро, описва поведението на идеален газ; по-специално в затворен контейнер, подложен на промени в обема, упражняван от механична сила.
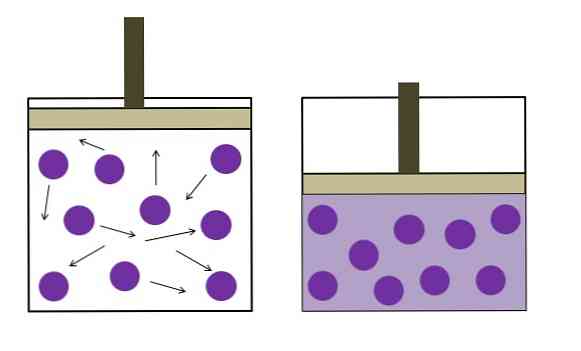
Горното изображение накратко обобщава закона Бойл-Мариот.
Пурпурните точки представляват молекули или газови атоми, които се сблъскват с вътрешните стени на контейнера (вляво). Чрез намаляване на наличното пространство или обем на контейнера, зает от този газ, се увеличават сблъсъците, което води до увеличаване на налягането (вдясно).
Това показва, че налягането Р и обемът V на газа са обратно пропорционални, ако контейнерът е херметически затворен; в противен случай по-високо налягане би било равно на по-голямо разширяване на контейнера.
Ако се направи графика V срещу P, с данните на V и P на Y и X оси, съответно, ще се наблюдава асимптотична крива. Колкото по-малък е V, толкова по-голямо е увеличението на P; това означава, че кривата ще се простира до високи стойности на Р по оста Х.
Разбира се, температурата остава постоянна; но ако един и същ експеримент се проведе при различни температури, относителните позиции на тези криви V срещу P биха се променили в декартовата ос. Промяната би била още по-очевидна, ако бъде нанесена на триизмерна ос, с константа Т на оста Z.
индекс
- 1 История на закона на Бойл
- 1.1 Контекст
- 1.2 Експериментирайте с живак
- 1.3 Edme Mariotte
- 1.4 Укрепване на закона
- 2 От какво се състои този закон??
- 3 Математически израз
- 4 За какво е предназначен? Какви проблеми решава законът на Бойл??
- 4.1 Парни машини
- 4.2 Sip напитки
- 4.3 Дихателна система
- 5 Примери (експерименти)
- 5.1 Експеримент 1
- 5.2 Експеримент 2
- 6 Препратки
История на закона на Бойл
фон
Тъй като ученият Галилео Галилей изразил вярата си в съществуването на празнота (1638), учените започнали да изучават свойствата на въздуха и частичните кухини..
Англо-ирландският химик Робърт Бойл започва изучаването на въздушните си свойства през 1638 г., след като научава, че Ото фон Герике, немски инженер и физик, е построил въздушна помпа..
Експериментирайте с живак
За да проведе изследванията си за налягането на въздуха, Бойл използва стъклена тръба във формата на "J", чиято конструкция се приписва на Робърт Хук, помощник на Бойл. Краят на късата ръкава беше запечатан, а краят на дългата ръка на тръбата беше отворен, за да постави живака.
От самото начало Бойл искаше да изучи еластичността на въздуха, качествено и количествено. Чрез изливане на живак през отворения край на тръбата с форма на "J", Бойл заключи, че въздухът в късата ръкава на тръбата се свива под налягане на живак.
резултати
Колкото по-голямо е количеството на живака, добавено към тръбата, толкова по-голямо е налягането на въздуха и по-малкия му обем. Бойл е получил отрицателен експоненциален график на обема на въздуха като функция на налягането.
Докато, ако начертаете обема на въздуха срещу обратното на налягането, имате права линия на положителния наклон.
През 1662 г. Бойл публикува първия физически закон, който е даден под формата на уравнение, което показва функционалната зависимост на две променливи. В този случай, налягането и обемът.
Бойл посочи, че е налице обратна връзка между натиска, упражняван върху газ, и обема, зает от този газ, като това съотношение е относително вярно за истинските газове. Повечето газове се държат като идеални газове при умерено налягане и температури.
При по-високи налягания и по-ниски температури отклоненията от поведението на реалните газове на идеалите стават по-забележими.
Edme Mariotte
Френският физик Едм Мариотт (1620-1684) самостоятелно открил същия закон през 1679 г. Но той имал заслуга да покаже, че обемът варира в зависимост от температурата. Ето защо се нарича Законът на Мариот или Законът на Бойл и Мариот.
Укрепване на закона
Даниел Бернули (1737) укрепи закона на Бойл, като посочи, че налягането на газ се произвежда от въздействието на газови частици върху стените на контейнера, които го съдържат..
През 1845 г. Джон Уотърстън публикува научна статия, в която се фокусира върху основните принципи на кинетичната теория на газовете.
По-късно, Рудолф Клаузиус, Джеймс Максуел и Лудквиг Болцман консолидираха кинетичната теория на газовете, която свързва налягането, упражнявано от газ с скоростта на частиците на газа в движение.
Колкото по-малък е обемът на контейнера, съдържащ газ, толкова по-голяма е честотата на въздействията на частиците, които я образуват срещу стените на контейнера; и следователно, по-голямото налягане, упражнявано от газа.
От какво се състои този закон??
Експериментите, извършени от Бойл, сочат, че има обратна връзка между обема, зает от газ и натиска върху него. Въпреки това, гореспоменатата връзка не е напълно линейна, както е показано от графика на изменението на обема според натиска, приписван на Бойл..
В Закона на Бойл е посочено, че обемът, зает от газ, е обратно пропорционален на налягането. Също така е показано, че произведението на налягането на газ от неговия обем е постоянно.
Математически израз
За да стигнем до математическия израз на закона Бойл-Мариот, започваме от:
V α 1 / P
Където това показва, че обемът, зает от газ, е обратно пропорционален на неговото налягане. Въпреки това, има една константа, която диктува колко обратно пропорционална е тази връзка.
V = k / P
Където k е константата на пропорционалност. Изчистване на k, което имате:
VP = k
Продуктът на налягането на газ от неговия обем е постоянен. след това:
V1P1 = k и V2P2 = k
От това може да се заключи, че:
V1P1 = V2P2
Последното е крайният израз или уравнение за закона на Бойл.
За какво е? Какви проблеми решава законът на Бойл??
Парни машини

Законът на Boyle-Mariotte се прилага за експлоатацията на парните машини. Това е двигател с външно горене, който използва преобразуването на топлинна енергия от количество вода в механична енергия.
Водата се загрява в херметически затворен котел, а получената пара оказва натиск съгласно закона Бойл-Мариоте, който произвежда обемно разширение на цилиндъра чрез натискане на бутало.
Линейното движение на буталото се преобразува в ротационно движение чрез използване на система от колена и колена, която може да задвижва колелата на локомотива или ротора на електрически генератор..
Понастоящем алтернативният парен двигател е малко използван двигател, тъй като той е изместен от електродвигателя и двигателя с вътрешно горене в транспортните средства..
Пият напитки
Действието на смучене на безалкохолна напитка или сок от бутилка през пластмасова тръба е свързано със закона Бойл-Мариот. Когато въздухът се изсмуква от тубата, използвайки устата, намалява налягането вътре в тръбата.
Този спад на налягането улеснява движението на течността в тръбата нагоре, позволявайки поглъщането му. Същият този принцип действа при извличането на кръв с помощта на спринцовка.
Дихателна система
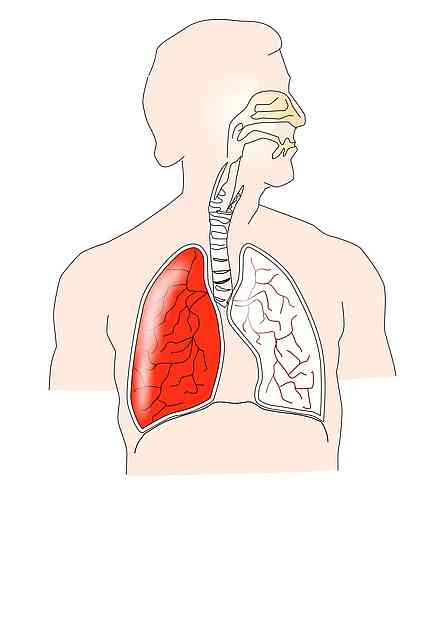
Законът на Бойл-Мариот е тясно свързан с функционирането на дихателната система. По време на вдъхновяващата фаза се случва свиване на диафрагмата и други мускули; например, външните междуредови, които предизвикват разширяване на гръдния кош.
Това води до намаляване на интраплевралното налягане, което причинява белодробно разширение, което води до увеличаване на обема на белите дробове. Следователно вътрепулмоналното налягане намалява според това, което е посочено в закона на Бойл-Мариот.
Когато вътрепулмоналното налягане е субатмосферно, атмосферният въздух се влива в белите дробове, което води до повишено налягане в белите дробове; равномерно, налягането му към атмосферното налягане и приключването на фазата на вдъхновение.
Впоследствие инспираторните мускули се отпускат и мускулите на издишване се свиват. Освен това, възниква белодробна еластична ретракция, явление, което предизвиква намаляване на обема на белите дробове, с последващо повишаване на вътрепулмоналното налягане, което може да се обясни със закона на Бойл-Мариот..
Чрез увеличаване на вътреплазменото налягане и увеличаване на атмосферното налягане въздухът изтича от вътрешността на белите дробове в атмосферата. Това става, докато налягането се изравни, което завършва фазата на изтичане.
Примери (експерименти)
Експеримент 1
Малък балон се поставя плътно затворен, като в устата му се поставя възел, в спринцовка, към която е извадено буталото, приблизително 20 ml. Буталото на спринцовката се поставя към средната част на спринцовката, иглата се отстранява и входящият отвор за въздух се запушва.
наблюдение
Чрез бавно издърпване на буталото на инжектора се забелязва, че балонът се надува.
обяснение
На стената на балона се упражняват два налягания: натиск върху вътрешната му страна, продукт на въздуха, съдържащ се в балона, и друго налягане върху външната повърхност на балона, упражняван от съдържащия се в спринцовката въздух..
При издърпване на буталото на инжектора в него се създава полу-вакуум. Следователно, налягането на въздуха върху външната страна на стената на помпата намалява, което прави налягането, упражнявано вътре в помпата, относително по-голямо..
Това нетно налягане, съгласно закона Бойл-Мариоте, ще доведе до разширяване на стената на балона и увеличаване на обема на балона.
Експеримент 2
Изрежете пластмасова бутилка, приблизително наполовина, като се уверите, че отрязъкът е възможно най-хоризонтален. В устата на бутилката се поставя добре регулиран балон, като в същото време в дълбоко ястие се поставя определено количество вода..
наблюдение
Чрез поставяне на дъното на бутилката с балона върху водата на съда, балонът е умерено напомпан.
обяснение
Водата измества определено количество въздух, увеличавайки налягането на въздуха върху стената на бутилката и вътрешността на балона. Това води, според закона на Бойл-Мариот, до увеличаване на обема на земното кълбо, което се визуализира от инфлацията на земното кълбо..
препратки
- Wikipedia. (2019). Законът на Бойл. Изтеглено от: en.wikipedia.org
- Редакторите на Encyclopaedia Britannica. (27 юли 2018 г.). Законът на Бойл. Енциклопедия Британика. Изтеглено от: britannica.com
- Хелменстина, Тод. (5 декември 2018 г.). Формулата на закона на Бойл. Изтеглено от: thoughtco.com
- Млади индийски филми. (15 май, 2018 г.). Законът на Бойл: Научен експеримент за деца. Възстановен от: yifindia.com
- Сесилия Бембибре (22 май 2011 г.). Балон с горещ въздух Определение ABC. Взето от: definicionabc.com
- Ganong, W, F. (2003). Медицинска физиология (19-то издание). Редакция на съвременния наръчник.


