Химическа структура, свойства и употреба на пропилена
на пропилей или пропен при стайна температура и при атмосферно налягане е в газообразно състояние и, подобно на други алкени, е безцветен. Той има миризма, подобна на маслото, но с по-малка интензивност. Той има диполен момент, тъй като макар да няма силна полярна връзка, неговата молекула е асиметрична.
Също, пропиленът е структурен изомер на циклопропан (те имат една и съща химична формула С)3Н6). Той се среща в природата като следствие от процесите на растителност и ферментация. Изкуствено възниква по време на преработката на изкопаеми горива като нефт, природен газ и в по-малка степен въглерод.

По същия начин, етиленът и пропиленът са продукти от рафиниране на нефт в процес на разделяне на големи въглеводородни молекули за генериране на малки въглеводороди с голямо търсене..
Пропиленът може да бъде получен и при използване на различни методологии:
- Реакция на обратимо етилен и бутен, където двойните връзки са счупени и преформулирани до получаване на пропилен.
- Чрез процес на дехидрогениране (загуба на водород) на пропан.
- Като част от програма за производство на олефини от метанол (МТО), пропиленът се произвежда от метанол. Това преминава през цеолитния катализатор, който подпомага дехидратацията му и води до образуването на етилен и пропилен..
3CH3ОН (метанол) => СН3СН = СН2 (пропилен) + ЗН2О (вода)
индекс
- 1 Химическа структура
- 2 Свойства
- 2.1 Молекулно тегло
- 2.2 Точка на кипене
- 2.3 Точка на топене
- 2.4 Точка на запалване
- 2.5 Разтворимост
- 2.6 Разтворимост, изразена като маса
- 2.7 Плътност
- 2.8 Плътност на парите
- 2.9 Налягане на парите
- 2.10 Самозапалване
- 2.11 Вискозитет
- 2.12 Топлина на горене
- 2.13 Изпарителна топлина
- 2.14 Повърхностно напрежение
- 2.15 Полимеризация
- 2.16 Точка на замръзване
- 2.17 Праг на мириса
- 3 Използване
- 3.1 Полипропилен
- 3.2 Акрилонитрил
- 3.3 Пропиленов оксид
- 3.4 За синтез на алкохоли и други приложения
- 4 Препратки
Химическа структура
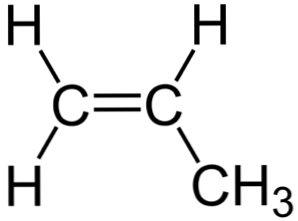
В изображението по-горе може да се види химическата структура на пропилена, в която се откроява неговата асиметрия (дясната страна е различна от лявата). Неговият въглероден скелет, без да включва атомите Н, може да се наблюдава като бумеранг.
Този бумеранг представлява една ненаситена или двойна връзка на една от страните (С1и следователно е плосък поради sp хибридизацията2 от въглеродни атоми.
Обаче другата страна е заета от метиловата група (-СН3), чиято хибридизация е sp3 и има тетраедрична геометрия. Така, гледано отпред, бумерангът е плосък, като атомите на Н изпъкват от това при приблизително 109,5 °.
В газовата фаза молекулата взаимодейства слабо с другите чрез дисперсионни сили. Също така взаимодействията между двойните връзки (π-π) на две пропиленови молекули се предотвратяват от метиловата група.
Това води до намаляване на техните междумолекулни сили, което се отразява в техните физични свойства. Само при много ниски температури пропиленът може да приеме твърда структура, в която бумеранът остава групиран с техните слаби взаимодействия.
свойства
Това е безцветен газ с ароматна миризма. Той се транспортира под формата на втечнен газ и когато излиза от контейнерите, които го съдържат, той го прави под формата на газ или течност. При ниски концентрации той образува експлозивна и запалима смес с въздуха, като плътността на пропилена е по-висока от тази на въздуха.
Молекулно тегло
42,081 g / mol
Точка на кипене
53,9 ° F до 760 mmHg
48 ° С до 760 mmHg
Точка на топене
301,4 ° F
185 ° С
Точка на възпламеняване
162 ºF
разтворимост
44,6 ml / 100 ml във вода.
1,250 ml / 100 ml в етанол.
524.5 ml / 100ml в оцетна киселина.
Разтворимост, изразена като маса
200 mg / l 25 ° С
плътност
0.609 mg / ml при -52.6 ° F
0.5139 при 20 ° С
Плътност на парите
1.46 до 32 ° F (спрямо въздуха, взет като еталон).
1,49 (въздух = 1).
1,91 kg / m3 до 273.15 ºK
Парно налягане
1 mmHg при -205,4 ° F
760 mmHg до -53.9 ° F
8,69 × 103 mmHg при 25 ° С (екстраполирана стойност).
1,158 kPa при 25 ° С
15.4 атм при 37 ° С
самозапалване
851 ° F
455 ° С
вискозитет
83,4 микропореста при 16,7 ° С.
Топлина на горене
16,692 BTU / lb
10.940 кал / г
Изпарителна топлина
104,62 cal / g (при температурата на кипене)
Повърхностно напрежение
16,7 дина / см при 90 ° С
полимеризация
Полимеризира при високи температури и високи налягания в присъствието на катализатори.
Точка на замръзване
185,25 ° С.
Праг на мирис
10-50 mg / m3 (Откриване)
100 mg / m3 (Разпознаване)
приложения

Използва се в нефтохимическата промишленост като гориво и алкилиращо средство. В химическата промишленост той се използва като суровина за производството и синтеза на множество производни.
Използва се предимно в производството на полипропилен, акрилонитрил (ACN), пропиленоксид (PO), алкохоли, кумол и акрилни киселини..
полипропилен
Полипропиленът е един от основните пластмасови материали, които се използват в електрониката и електрическите аксесоари, домакински изделия, капачки за бутилки и куфари.
Ламинираният материал се използва при опаковането на сладкиши, етикети, компактдискове и др., Докато влакната са направени от папки и дрехи..
акрилонитрил
Еластомерни полимери и влакна се получават от акрилонитрил. Тези влакна са предназначени за производство на различни форми на облекло, като например пуловери, чорапи и спортни дрехи. Използват се и в домашни мебели, в папки, тапицерии, възглавници и одеяла.
Пропиленов оксид
Пропиленов оксид участва като компонент в синтеза на полиуретан. Той се използва при производството на гъвкава пяна и твърда пяна. Гъвкавата пяна се използва като пълнител за домашни мебели и в автомобилната индустрия.
От друга страна, твърдата пяна се използва главно като изолационен материал за сгради.
В допълнение, пропиленоксид се използва при производството на пропиленгликол. Това съединение се използва при производството на ненаситени полиестерни смоли и като антифриз.
В допълнение, пропиленоксид се използва при производството на пропиленгликол етер. Този етер има приложение при производството на бои, дрехи, мастила, смоли и почистващи препарати.
За синтез на алкохоли и други приложения
Пропиленът позволява получаването на някои алкохоли, сред които изопропанол, използван като разтворител в козметиката и продуктите за лична хигиена. Освен това той изпълнява функцията на антисептично средство.
- Изопропанолът участва в производството на бои, смоли, мастила и самозалепващи ленти. Използва се и във фармацевтичната индустрия.
- Оксо-алкохол2-етилхексанол се използва при производството на фталати, пластификатори, лепила и бои..
- Бутанолът се използва в производството на бои, покрития, смоли, багрила, фармацевтични продукти и полимери.
От друга страна, кумолът се произвежда от комбинацията от пропилен и бензол. Куменът е основното съединение в производството на фенол и ацетон, използвани в различни продукти, като поликарбонати, фенолни смоли, епоксидни смоли и метилметакрилат..
Накрая, акриловата киселина - друг продукт, получен от пропилен - се използва в производството на акрилни естери и смоли за бои, покрития и лепила..
препратки
- Михал Осменда (26 декември 2007 г.). Запали огъня ми. [Фигура]. Възстановен на 23 май 2018 г. от: commons.wikimedia.org
- Групата Linde. (2018). Пропилен. Възстановен на 23 май 2018 г. от: linde-gas.com
- Wikipedia. (2018). Пропен. Възстановен на 23 май 2018 г. от: en.wikipedia.org
- PubChem. (2018). Пропилен. Възстановен на 27 май 2018 г. от: pubchem.ncbi.nlm.nih.gov
- Весович Велиса. (7 февруари 2011 г.). Пропилен. Възстановен на 27 май 2018 г. от: thermopedia.com
- Джефри С. Плоткин. (08 август 2016 г.). Пропиленовият проблем. Възстановен на 27 май 2018 г. от: acs.org
- ICIS. (6 ноември 2017 г.). Използва се пропилен и пазарни данни. Възстановен на 27 май 2018 г. от: icis.com


