Екзотермичен реакционен процес, типове и примери
на екзотермична реакция е вид химическа реакция, при която се осъществява пренос на енергия, главно под формата на отделяне на топлина или светлина. Името идва от гръцката префикс екзо, което означава "в чужбина"; и терминът "термичен", който се отнася до топлина или температура.
В този смисъл екзотермичните реакции могат да пренесат други видове енергия в средата, в която се генерират, като например с експлозии и техния начин на прехвърляне на кинетична и звукова енергия, когато вещества, които са в газообразна фаза при високи температури, се разширяват. насилствен начин.
По същия начин, в случай на използване на батерии, се извършва и екзотермична реакция, само в този случай се пренася електрическа енергия..
индекс
- 1 Процес
- 2 вида
- 2.1 Реакции на горене
- 2.2 Реакции на неутрализация
- 2.3 Реакции на окисляване
- 2.4 Термитна реакция
- 2.5 Реакционна полимеризация
- 2.6 Реакция на ядрено делене
- 2.7 Други реакции
- 3 Примери
- 4 Препратки
процес
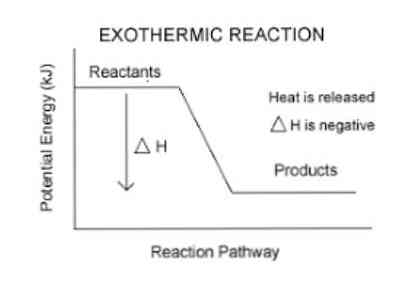
По-рано беше споменато, че когато настъпи екзотермична реакция, настъпва отделяне на енергия, което може да бъде визуализирано по-лесно в следното уравнение:
Реагенти (и) → Продукт (и) + Енергия
За да се определи количествено енергията, погълната или освободена от системата, се използва термодинамичен параметър, наречен енталпия (обозначен с "Н"). Ако в дадена система (в този случай химическа реакция) има отделяне на енергия в околността, тогава изменението на енталпията (изразено като ΔH) ще има отрицателна стойност.
В противен случай, ако изменението на тази мярка е положително, то отразява усвояването на топлината от околностите. Също така, величината на енталпийната вариация на системата е израз на количеството енергия, което се прехвърля към или от околната среда..
Колкото по-голяма е величината на ΔH, толкова по-голямо е отделянето на енергия от системата към заобикалящата среда.
Това е така, защото в тези реакции нетната енергия, която се освобождава, когато се създават нови връзки, е по-голяма от нетната енергия, използвана при фрагментирането на връзките.
От гореизложеното може да се заключи, че този вид реакции са много чести, тъй като продуктите от реакцията имат количество енергия, съхранено в връзките, което е по-голямо от това, което се съдържа в реагентите..
тип
Има различни видове екзотермични реакции в различните области на химията, независимо дали в лабораторията или в промишлеността; някои се извършват спонтанно, а други се нуждаят от специфични условия или от някакъв вид вещество, като например катализатор.
Следните са най-важните видове екзотермични реакции:
Горивни реакции
Реакциите на горене са тези на окислително-редукционния тип, които се появяват, когато едно или повече вещества реагират с кислород, като обикновено водят до отделяне на светлина и топлинна енергия, което е светлина и топлина, когато се произвежда пламък..
Реакции на неутрализация
Реакциите на неутрализация се характеризират с взаимодействието между киселинен вид и алкална субстанция (основа) за образуване на сол и вода, които проявяват екзотермична природа..
Реакции на окисляване
Има много реакции от този тип, които показват екзотермично поведение, тъй като окисляването на кислорода причинява отделянето на голямо количество енергия, както се случва при окислението на въглеводороди..
Термитна реакция
Тази реакция може да доведе до температура около 3000 ° C и поради високия афинитет на алуминиевия прах с голям брой метални оксиди, се използва при заваряване на стомана и желязо..
Реакция на полимеризация
Този тип реакция е този, който възниква, когато определен брой химически видове, наречени мономери, реагират, които са единици, които, когато се комбинират, се повтарят в вериги за образуване на макромолекулни структури, наречени полимери.
Реакция на ядрено делене
Този процес се отнася до разделяне на ядрото на атом, считан за тежък - т.е. с масов номер (А) по-голям от 200 - за получаване на фрагменти или ядра с по-малък размер с междинна маса..
В тази реакция, където се образуват един или повече неутрони, се отделя голямо количество енергия, тъй като сърцевината с по-голямо тегло има по-ниска стабилност, отколкото нейните продукти..
Други реакции
Има и други екзотермични реакции от голямо значение, като дехидратация на някои въглехидрати при реакция със сярна киселина, абсорбция на вода, която има натриев хидроксид, изложена на открито или окисляването на метални видове при много корозионни реакции..
Примери
По-долу са дадени някои примери за екзотермични реакции, които водят до промяна на енталпията, която има отрицателна стойност поради факта, че те освобождават енергия, както е споменато по-горе..
Например, изгарянето на пропан е спонтанна екзотермична реакция:
C3Н8(g) + 5 °2(g) → 3CO2(g) + 4Н2O (l)
Друг случай на екзотермично поведение се показва чрез реакцията на неутрализация между натриев карбонат и солна киселина:
разтвор на натриев бикарбонат3(ac) + HCl (ac) - NaCl (ac) + H2О (1) + СО2(G)
Представено е и окислението на етанол до оцетна киселина, използвано в аерозолите, чиято пълна реакция е показана в следното уравнение:
3CH3СН2OH + 2K2Cr2О7 + 8Н2SW4 → CH3СООН + 2Cr (SO4)3 + 2K2SW4 + 11Н2О
Друг клас екзотермична реакция е т.нар. Термитна реакция, при която алуминият се комбинира с метален оксид, както е показано по-долу:
2Al (и) + Вяра2О3(s) → Al2О3s) + Fe (l)
В допълнение към описаните по-горе примери, има голямо разнообразие от реакции, които също се считат за екзотермични, като разлагане на някои органични отпадъчни вещества за компостиране..
Той също така подчертава окислението на луцифериновия пигмент чрез действието на ензима луцифераза, за да произведе биолуминесценцията, характерна за светулките, и дори дишането, както и много други реакции..
препратки
- Wikipedia. (Н.О.). Екзотермична реакция. Изтеглено от es.wikipedia.org
- Би Би Си. (Н.О.). Енергийни промени и обратими реакции. Изтеглено от bbc.co.uk
- Chang, R. (2007). Химия, Девето издание. (McGraw-Hill).
- Walker, D. (2007). Химични реакции. Получено от books.google.co.ve
- Saunders, N. (2007). Изследване на химични реакции. Получено от books.google.co.ve


