Химическа структура, свойства и употреба на амониев сулфат
на амониев сулфат Това е тройна и амонячна неорганична сол на сярната киселина. Неговата химична формула е (NH4)2SW4. Следователно стехиометричните пропорции казват, че за всеки сулфатен анион има две взаимодействащи с него амониеви катиони. Това позволява неутралността на солта ((+1) + 2 + (-2)).
Нейната номенклатура се дължи на факта, че тя е сол, получена от Н2SW4, промяна на суфикса "uric" на "ato". По този начин двете първоначални протони се заменят с NH4+, реакционен продукт с амоняк (NH3). След това химичното уравнение за неговия синтез е: 2 NH3 + Н2SW4 = NH4)2SW4
Амониевият сулфат е магазин за азот и сяра, както незаменим в химията на почвите и торовете.
индекс
- 1 Химическа структура
- 2 Физични и химични свойства
- 2.1 Молекулно тегло
- 2.2 Физически вид
- 2.3 Миризма
- 2.4 Точка на топене
- 2.5 Разтворимост
- 2.6 Плътност
- 2.7 Налягане на парите
- 2.8 Точка на запалване
- 2.9 рН
- 2.10 Стабилност
- 2.11 Разлагане
- 2.12 Корозия
- 3 Използване
- 3.1 В селското стопанство
- 3.2 Като аналитичен реагент
- 3.3 При утаяване и изолиране на протеини
- 3.4 В индустрията
- 3.5 Други приложения
- 4 Препратки
Химическа структура
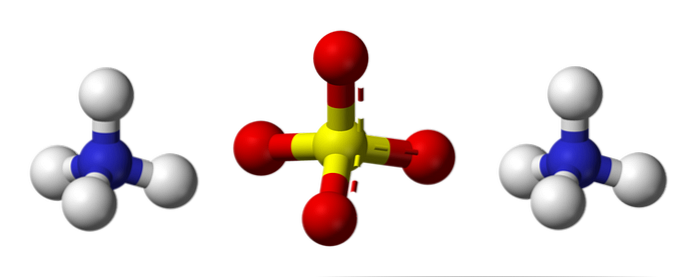
Горното изображение илюстрира молекулярните геометрии на NH йони4+ и SO42-. Червените сфери отговарят на кислородните атоми, белите сфери съответстват на водородните атоми, сините сфери на азотния атом и жълтите сфери съответстват на серен атом..
И двата йона могат да се разглеждат като два тетраедъра, като по този начин имат три единици, които взаимодействат, за да образуват орторомбична структура на кристалите. Сулфат-анионът е SO42- и е в състояние да дарява или приема четири водородни връзки, точно като NH катиона4+.
Физични и химични свойства
Молекулно тегло
132,134 g / mol.
Физически вид
Твърдо бяло. Орторомбични бели или кафяви кристали, в зависимост от нивата на примесите.
миризма
тоалетна.
Точка на топене
280 ° С. Тази точка на топене, ниска в сравнение с други йонни съединения, се дължи на факта, че тя е сол с моновалентни катиони (+1) и с различни йони в размерите си, което води до ниска кристална ретикуларна енергия..
разтворимост
76,4 g / 100 g вода при 25 ° С. Този афинитет към водата се дължи на големия капацитет на неговите молекули да солватират амониеви йони. От друга страна, той е неразтворим в ацетон и алкохол; т.е. в разтворители, по-малко полярни от вода.
плътност
1.77 g / cm3 при 25 ° С.
Парно налягане
1,871 kPa при 20 ° C.
Точка на запалимост
26 ° С.
рН
5,0-6,0 (25 ° С, 1 М разтвор). Леко киселото рН се дължи на хидролизата на NH4+ във вода, като се получава Н3О+ при ниски концентрации.
стабилност
Стабилен в подходящи условия на околната среда. При контакт със силни оксиданти могат да се запалят.
разлагане
Той започва да се разлага при 150 ° С, освобождавайки токсични пари на серен оксид, азотен оксид и амоняк.
корозия
Не атакува желязо или алуминий.
приложения

В селското стопанство
- Амониевият сулфат се използва като тор в алкални почви. Амониевата сол има 21% азот и 24% сяра в състава си. Обаче, съществуват съединения, които осигуряват по-голямо количество азот, отколкото амониевия сулфат; Предимството на последното е високата му концентрация на сяра.
- Сярата е от съществено значение за синтеза на протеини, тъй като няколко аминокиселини - като цистин, метионин и цистеин - притежават сяра. Поради тези причини амониевият сулфат продължава да бъде един от най-важните торове.
- Използва се в посевите от пшеница, царевица, ориз, памук, картофи, коноп и овощни дървета.
- Ниско рН на алкални почви поради техния принос в процеса на нитрификация, извършван от микроби. Използва се амониев (NH)4+) за производство на нитрати (NO3-) и се освобождава Н+: 2NH4+ + 4о2 => 2NO3- + 2H2О + 4Н+. Увеличаването на концентрацията на водород намалява рН на алкалните почви и позволява по-голяма употреба.
- В допълнение към използването му като тор, амониевият сулфат действа като коадювант за разтворими инсектициди, хербициди и фунгициди, които се пръскат върху култури..
- Сулфатът е способен да отделя присъстващите йони в почвата и в напоителната вода, които са необходими за живота на някои патогени. Сред йоните, които улавят амониевия сулфат, са Са2+, Mg2+, Вярата2+ и вярата3+. Това действие повишава микробицидния ефект на споменатите агенти.
Като аналитичен реагент
Амониевият сулфат действа като преципитиращ агент в електрохимичния анализ, в микробиологична културална среда и при получаването на амониеви соли.
При утаяване и изолиране на протеини
Амониевият сулфат се използва за изолиране и пречистване на протеини, особено на плазмени протеини. Към плазмата се добавя количество амониев сулфат до определена концентрация; по този начин се причинява утаяване на група протеини.
Утайката се събира чрез центрофугиране и към супернатантата се добавя допълнително количество амониев сулфат и при нова концентрация настъпва утаяване на друга група протеини..
Повторението на предишния процес в последователна форма позволява получаването на различни фракции от плазмените протеини.
Преди да се появят новите технологии на молекулярната биология, тази процедура позволява изолирането на плазмените протеини от голямо значение в медицината, например: имуноглобулини, коагулационни фактори и др..
В индустрията
Амониевият сулфат действа, за да забави началото на пожара в текстилната индустрия. Използва се като добавка в галваничната индустрия. Използва се и при производството на водороден пероксид, амониев хлорид и др..
Други приложения
- Амониевият сулфат се използва като регулиращ агент за осмотично налягане и като средство за утаяване на сол.
- Във формата на амониев лаурилсулфат, повърхностното напрежение на водата намалява, като по този начин позволява отделянето на замърсители чрез увеличаване на твърдостта на водата.
- Той е антикорозионен агент.
- Използва се като хранителна добавка, която регулира киселинността в брашното тесто и хляба.
препратки
- ОИСР SIDS. (Октомври 2004 г.). Амониев сулфат. [PDF]. Възстановен на 27 април 2018 г. от: inchem.org
- Мозаичната компания. (2018). Амониев сулфат. Възстановен на 27 април 2018 г. от: cropnutrition.com
- Wikipedia. (2018). Амониев сулфат. Възстановен на 27 април 2018 г. от: en.wikipedia.org
- PubChem. (2018). Амониев сулфат. Възстановен на 27 април 2018 г. от: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23 юли 2015 г.). [Фигура]. Възстановен на 27 април 2018 г. от: flickr.com
- Паула Пап (22 февруари 2017 г.). Приложения и приложения на амониев сулфат. Възстановен на 27 април 2018 г. от: business.com


