Формула на натриев ацетат, подготовка, свойства, рискове и употреба
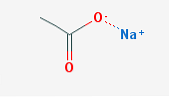
на натриев ацетат, известен също като натриев етаноат (съкратено NaOAc), е натриева сол на оцетната киселина. Химичната му формула е СН3COONa и има йонна връзка между натриевия йон и ацетатния йон.
Това химично съединение присъства естествено в растителните и животински тъкани. Може да се намери във всякаква форма, безводна или трихидратирана. И двете йони, Na + и СН3COO- присъстват в организмите и изпълняват жизнени функции: натриевият йон като регулатор на общата вода в тялото и ацетатен йон като акцептор на водород (Формула на натриевия ацетат, 2005-2017).
индекс
- 1 Подготовка
- 2 Физични и химични свойства
- 3 Реактивност и опасности
- 4 Работа и съхранение
- 5 Употреби и приложения
- 6 Препратки
подготовка
Натриевият ацетат е съединение, което може да бъде приготвено по прост и достъпен начин за всеки. Обикновено неговото приготвяне е известно като "експеримент за горещ лед", тъй като кристализацията прилича на вода в твърдо състояние (учен, 2016).
За приготвяне на натриев ацетат се нуждаете само от оцет (оцетна киселина) и натриев карбонат или натриев бикарбонат. Просто добавете бикарбоната към оцета, произвеждайки ефервесцентна реакция, тъй като освобождава въглероден диоксид според реакциите.
СН3СООН + NaHCO3 → CH3COONa + Н2CO3
Н2CO3 → CO2 + Н2О
Карбонатът или натриевият бикарбонат могат да бъдат заместени с натриев хидроксид (луга), където се получават натриев ацетат и вода съгласно реакцията:
СН3СООН + NaOH → CH3COONa + Н2О
Тази реакция не предизвиква ефервесценция, но има недостатъка, че натриевият хидроксид е по-труден за обработка, отколкото бикарбонатен.
За да се получи ефектът от кристализацията (или ефекта на горещия лед), разтворът трябва да бъде пренаситен чрез нагряване, за да се разтвори бикарбонатът в излишък. Затвореният контейнер след това се охлажда и след това се прекристализира. След това кристалите се филтрират и разпрашават за съхранение (обезкостяване, S.F.).
Физични и химични свойства
Натриевият ацетат е бяло хигроскопично стъкло с миризма на оцет.

В случая на безводна форма на съединението, тя има молекулно тегло от 82.03 g / mol и плътност е 1.5 g / ml. Точката на топене е 324 градуса по Целзий, а точката на кипене е 881,4 градуса по Целзий.
В своята трихидратна форма, тя има молекулно тегло 136,03 g / mol и плътност 1,45 g / ml. Точките на топене и кипене намаляват драстично до 58 градуса по Целзий и съответно до 122 градуса по Целзий.
Натриевият ацетат е много разтворим във вода. Разтворимостта на трихидратната форма е 46.5 g натриев ацетат в 100 ml вода при 20 градуса по Целзий и в безводна форма може да се разтвори 123 грама на 100 ml вода (Национален център за биотехнологична информация, 2017). ).
И двете форми са разтворими в ацетон, метанол, хидразин и трихидратната форма е разтворима в етанол. Натриевият ацетат има моноклинна кристална структура (Royal Society of Chemistry, 2015).
Натриевият ацетат е конюгатната основа на оцетната киселина, така че можете да използвате разтвор на оцетна киселина / натриев ацетат за приготвяне на буферни разтвори, за да се контролира рН.
Разтворът на натриев ацетат във вода е слабо алкален. Когато топлината е по-висока от 324 градуса по Целзий, тази сол се разлага, като произвежда дим с оцетна киселина.
Реактивност и опасности
Натриевият ацетат се класифицира като стабилно съединение и несъвместим с окислителни агенти. При нагряване може да се получат пари от оцетна киселина и освобождаване на СО2. Съединението може да бъде запалимо при високи температури, освобождаващи CO и CO2.
Безопасността на натриевия ацетат е обстойно изследвана в животински модели на плъхове и мишки. Когато се прилага орално, леталната доза, която убива половината от популацията от плъхове, е 3530 mg натриев ацетат на килограм телесно тегло на плъх..
Ако се вдишат вместо приема, дозата, необходима за убиване на половината от популацията от плъхове, е много по-висока, повече от 30 g / m3 на час..
При мишки, подкожно или подкожно инжектиране на 3200 mg / kg телесно тегло ще убие половината от популацията от мишки, подобно на поглъщането на натриев ацетат при плъхове..
Но при мишки, когато се дават орално, те могат да издържат много повече от плъховете; като летална доза за половината от популацията на мишки с 6891 mg / kg телесно тегло.
При хора вдишването на натриев ацетат може да предизвика кашлица и възпалено гърло, докато директният контакт на кожата или очите може да предизвика зачервяване и дразнене. Въпреки това, и като цяло, токсичността при хората е минимална (WASSERMAN, 2015).
Той може да предизвика дразнене на храносмилателния тракт с коремна болка, гадене, повръщане и да повлияе на отделителната система. Вдишването на съединението може да предизвика дразнене на дихателните пътища. Симптомите могат да включват кашлица, възпалено гърло, задух и болка в гърдите.
В случай на контакт с очите, контактните лещи трябва да бъдат проверени и отстранени. Очите трябва да се измият незабавно с обилно количество вода в продължение на най-малко 15 минути. Можете да използвате студена вода. При дразнене трябва да се получи медицинска помощ.
В случай на контакт с кожата, тя трябва да се измие със сапун и вода. Можете да използвате студена вода. Раздразнена кожа е покрита с омекотяващо средство. Както при контакт с очите, при развитие на дразнене трябва да се получи медицинска помощ.
Ако се вдиша, жертвата трябва да се премести на хладно място. Ако не диша, трябва да се приложи изкуствено дишане. Ако дишането е трудно, трябва да се осигури кислород. Още веднъж е необходимо незабавно да се потърси лекарска помощ.
В случай на поглъщане, не трябва да се предизвиква повръщане, освен ако изрично не е посочено от медицински персонал. Никога не давайте нищо през устата на лице в безсъзнание.
Разхлабените дрехи, като яка за риза, вратовръзка или колан, трябва да се разхлабят. Трябва да се получи медицинска помощ, ако се появят симптоми (Информационен лист за безопасност на натриев ацетат безводен, 2013).
Работа и съхранение
-Съединението трябва да се пази от топлина и източници на запалване
-Празните контейнери представляват опасност от пожар, остатъкът се изпарява под аспиратор
-Електрическото оборудване трябва да бъде заземено, за да се избегне искрене
-Не поглъщайте или вдишвайте прах
-Трябва да се носи подходящото защитно облекло
-В случай на липса на вентилация трябва да се носи подходящо оборудване за дишане
-В случай на поглъщане, трябва незабавно да отидете на лекар и да покажете контейнера или етикета
-Реагентът трябва да се пази от несъвместими вещества като окислители и киселини.
-Съдът да се съхранява плътно затворен, като контейнерът се държи на хладно и добре проветриво място.
Употреби и приложения
Натриевият ацетат се използва в изключително разнообразна гама от индустрии. В текстилната промишленост натриевият ацетат неутрализира отпадъчните потоци от сярна киселина, а също и като фоторезист, докато се използват анилинови багрила. Това подобрява качеството на готовите тъкани.
На снимката натриевият ацетат е част от разтвора на проявителя и действа като фоторезист. Натриевият ацетат се използва за намаляване на щетите, причинени от вода на бетон, като действа като уплътнител, като същевременно е екологично чист и по-евтин от обичайно използваната епоксидна алтернатива за уплътняване на бетона срещу проникване на вода..
Също така е и ецващо средство в хромовото дъбене и спомага за предотвратяване на вулканизацията на хлоропрена при производството на синтетичен каучук. При обработката на памук за памучни подложки за еднократна употреба, натриев ацетат се използва за премахване на натрупването на статично електричество.
Натриевият ацетат, прибавен към храната, действа като консервант и ароматизиращ агент. По-специално, картофените чипси с натриев ацетат имат отличителен вкус на сол и оцет.
Натриевият ацетат се използва също и в подгряващи възглавници, ръкавици и горещ лед. Кристалите на натриевия ацетат на трихидрат се стопяват при 58,4 ° С, като се разтварят в тяхната кристализационна вода.
Когато се нагрява над точката на топене и след това се оставя да се охлади, водният разтвор става пренаситен. Този разтвор може да се охлади до стайна температура, без да образува кристали.
Чрез натискане на метален диск в нагряващата подложка се образува център за нуклеация, който кара кристала да се кристализира обратно в твърд натриев ацетат трихидрат. Процесът на свързване на кристализацията е екзотермичен. Латентната топлина на сливане е приблизително 264-289 kJ / kg.
За разлика от някои видове топлинни опаковки, като тези, които зависят от необратими химични реакции, топлинен пакет от натриев ацетат може лесно да бъде използван отново чрез потапяне на опаковката в кипяща вода за няколко минути, докато кристалите се разтворят напълно и че опаковката се охлажда бавно, докато достигне стайна температура.
Разтворите на натриев ацетат и оцетна киселина действат като буфери за поддържане на относително постоянно рН, полезно свойство както за реакциите на биохимичните изследвания, така и за нефтената промишленост и в козметичната индустрия..
Натриевият ацетат може да се използва за утаяване на малки нуклеинови киселини. Това утаяване може да се използва за концентриране на малки нуклеинови киселини от разредени разтвори, такива като по-ниско функциониращ буфер след фракциониране на flashPAGE.
Когато по-малко от 2 μg от нуклеиновата киселина се зареждат в раздробяващата машина на flashPAGE, утаяването с натриев ацетат / етанол се препоръчва през нощта с носител, като линеен акриламид или гликоген, за максимално възстановяване на нуклеинова киселина от работещ буфер бавен.
Използването на гликоген като носител не се препоръчва за пробите, които ще се използват за анализ на ДНК чипове (натриево ацетатно утаяване на малки нуклеинови киселини, S.F.)..
В областта на медицината, разтвори на натриев ацетат лекуват пациенти с високи нива на кръвна киселина и / или ниски нива на натрий.
Натрият е основният катион на извънклетъчната течност. Съдържа повече от 90% от общия катион при нормална плазмена концентрация приблизително 140 mEq / l. Натриевият йон играе ключова роля в контрола на общата вода в тялото и неговото разпределение (Sodium Acetate, 2010).
Ацетат е акцептор на водородни йони. Той също така служи като алтернативен източник на бикарбонат (HCO3-) за метаболитна конверсия в черния дроб. Показано е, че това превръщане протича с лекота, дори при наличие на тежко чернодробно заболяване.
Инжектиране на натриев ацетат, разреден с вода, се дава интравенозно като електролитен пълнител. Всеки 20 ml съдържа 3,28 g натриев ацетат, което осигурява 40 mEq натрий (Na +) и ацетат (HCO)3-). Разтворът не съдържа бактериостат, антимикробен агент или добавен буфер. Може да съдържа оцетна киселина за регулиране на рН (рН е 6,5 (6,0 до 7,0)). Осмоларната концентрация е 4 mOsmol / ml (калций).
Смята се, че разтворът е алтернатива на натриевия хлорид, за да осигури натриев йон (Na +) за добавянето му към инфузионни течности с голям обем за интравенозно приложение (Sodium Acetate, 2009)..
Разтвори, съдържащи натриеви йони, трябва да се използват много внимателно, особено в случаи на пациенти със застойна сърдечна недостатъчност, тежка бъбречна недостатъчност и в клинични състояния, при които има оток с задържане на натрий..
При пациенти с нарушена бъбречна функция, прилагането на разтвори, съдържащи натриеви йони, може да доведе до задържане на натрий. Разтвори, съдържащи ацетатни йони, трябва да се използват много внимателно при пациенти с метаболитна или респираторна алкалоза.
Ацетатът трябва да се прилага много внимателно при състояния, при които се наблюдава повишаване на нивото или нарушената употреба на този йон, като тежка чернодробна недостатъчност..
препратки
- (S.F.). Как да направим натриев ацетат от домакински съставки. Recuperado de instructables: instructables.com.
- Информационен лист за безопасност Натриев ацетат безводен. (2013 г., 21 май). Изтеглено от sciencelab: sciencelab.com.
- Национален център за биотехнологична информация. (2017, 4 март). PubChem Compound Database; CID = 517045. Изтеглено от PubChem.
- Кралско химическо дружество. (2015). Натриев ацетат. Извлечено от chemspider.com.
- учен, D. N.-c. (2016, 12 август). "HOT ICE" - невероятен експеримент. Извлечено от youtube.com.
- Натриев ацетат. (2009, 19 май). Извлечено от rxlist.
- Натриев ацетат. (2010, април). Възстановен от drugs.com.
- Формула на натриевия ацетат. (2005-2017). Възстановен от softschools.com.
- Утаяване на натриев ацетат на малки нуклеинови киселини. (S.F.). Възстановен от термофисаря.
- WASSERMAN, R. (2015, 16 август). Какво е сол на натриев ацетат? Изтеглено от livestrong: livestrong.com.


