Амониева хидроксидна структура, свойства, номенклатура, приложения
на амониев хидроксид е съединение с NH молекулна формула4ОН или Н5НЕ произведени чрез разтваряне на амонячен газ (NH3) във вода. Поради тази причина той получава имената на амонячна вода или течен амоняк.
Това е безцветна течност с много интензивна и остра миризма, която не е изолираща. Тези характеристики имат пряка връзка с концентрацията на NH3 разтворени във водата; концентрация, която всъщност, като газ, може да покрие огромни количества от нея, разтворени в малък обем вода.
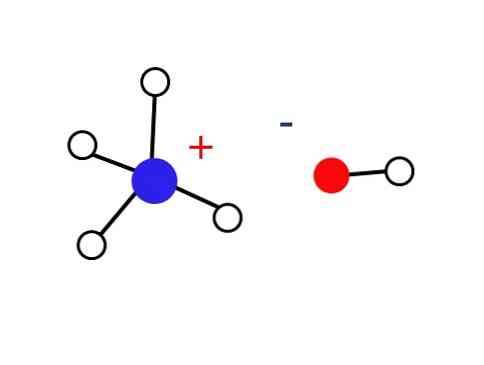
Значително малка част от тези водни разтвори се състои от NH катиони4+ и ОН аниони-. От друга страна, в много разредени разтвори или в замразени твърди вещества при много ниски температури амонякът може да се намери под формата на хидрати, като например:3Н2О, 2NH3Н2О и NH32Н2О.
Като любопитен факт облаците на Юпитер се образуват от разредени разтвори на амониев хидроксид. Пространствената сонда на Галилео обаче не успя да намери вода в облаците на планетата, което би могло да се очаква от знанието, че е известно образуването на амониев хидроксид; това са кристали на NH4OH напълно безводен.
Амониевият йон (NH4+) се произвежда в туморния бъбречен лумен чрез обединяване на амоняк и водород, секретирани от бъбречните тубулни клетки. По същия начин, амониевият се произвежда в бъбречните тубулни клетки в процеса на превръщане на глутамин в глутамат, и на свой ред, в превръщането на глутамата в а-кетоглутарат..
Амонякът се произвежда промишлено по метода на Хабер-Бош, в който се реагират азотните и водородните газове; използване на железен йон, алуминиев оксид и калиев оксид като катализатори. Реакцията се провежда при високи налягания (150-300 атмосфери) и високи температури (400-500 ° С), с добив 10-20%.
В реакцията се получава амоняк, който при окисляване произвежда нитрити и нитрати. Те са от съществено значение за получаване на азотна киселина и торове като амониев нитрат.
индекс
- 1 Химическа структура
- 1.1 Амонячен лед
- 2 Физични и химични свойства
- 2.1 Молекулна формула
- 2.2 Молекулно тегло
- 2.3 Външен вид
- 2.4 Концентрация
- 2.5 Миризма
- 2.6 Вкус
- 2.7 Стойност на прага
- 2.8 Точка на кипене
- 2.9 Разтворимост
- 2.10 Разтворимост във вода
- 2.11 Плътност
- 2.12 Плътност на парите
- 2.13 Парно налягане
- 2.14 Разяждащо действие
- 2.15 рН
- 2.16 Дисоциационна константа
- 3 Номенклатура
- 4 Разтворимост
- 5 Рискове
- 5.1 Реактивност
- 6 Използване
- 6.1 В храната
- 6.2 Терапевтични средства
- 6.3 Промишлени и разни
- 6.4 В селското стопанство
- 7 Препратки
Химическа структура
Както е посочено от неговото определение, амониевият хидроксид се състои от воден разтвор на амонячен газ. Следователно, вътре в течността няма определена структура, различна от тази на произволно подреждане на NH йони4+ и ОН- солватирани с водни молекули.
Амониевите и хидроксилните йони са продукти на равновесие на хидролиза на амоняк, така че е обичайно тези разтвори да имат остър мирис:
NH3(g) + Н2O (l) <=> NH4+(ac) + OH-(Воден)
Според химичното уравнение, високото понижаване на концентрацията на водата би изместило равновесието към образуването на повече амоняк; с нагряване на амониевия хидроксид се освобождават амонячни пари.
Поради тази причина, NH йони4+ и ОН- те не успяват да образуват кристал в земните условия, което води до следствие, че твърдата основа NH4ОН не съществува.
Това твърдо вещество трябва да се състои само от йони, взаимодействащи електростатично (както е показано на изображението).
Амонячен лед
Въпреки това, при температури под 0ºC и заобиколени от огромни налягания, като тези, които преобладават в ядрата на ледените луни, амонякът и замразяването на водата. По този начин те кристализират в твърда смес с разнообразни стехиометрични пропорции, като най-простият NH3Н2О: амонячен монохидрат.
NH3Н2О и NH32Н2Или те са амонячен лед, тъй като твърдото вещество се състои от кристална подредба на водни молекули и амоняк, свързан с водородни връзки..
Като се има предвид промяна на Т и Р, според изчислителни изследвания, които симулират всички физически променливи и тяхното въздействие върху този лед, настъпва преход на NH фаза.3. NH2Или до NH фаза4OH.
Ето защо, само в тези екстремни условия, NH4ОН може да съществува като продукт на протониране в леда между NH3 и Н2О:
NH3(s) + H2O (s) <=> NH4OH (s)
Имайте предвид, че този път, за разлика от хидролизата на амоняка, засегнатите видове са в твърда фаза. Амонячен лед, който става солен, без да отделя амоняк.
Физични и химични свойства
Молекулна формула
NH4ОН или Н5NO
Молекулно тегло
35,046 g / mol
вид
Това е безцветна течност.
концентрация
До около 30% (за NH йони4+ и ОН-).
миризма
Много силен и остър.
вкус
акър.
Стойност на прага
34 ppm за неспецифично откриване.
Точка на кипене
38 ºC (25%).
разтворимост
Съществува само във воден разтвор.
Разтворимост във вода
Смесва се в неограничени пропорции.
плътност
0.90 g / cm3 при 25 ° С.
Плътност на парите
В сравнение с въздуха, взет като единица: 0.6. Това означава, че е по-малко плътен от въздуха. Въпреки това, логически посочената стойност се отнася до амоняк като газ, а не до неговите водни разтвори или до NH4OH.
Парно налягане
2.160 mmHg при 25 ° С.
Разяждащо действие
Той е способен да разтваря цинк и мед.
рН
11.6 (разтвор 1 N); 11.1 (разтвор 0.1 N) и 10.6 (0.01 N разтвор).
Константа на дисоциация
pKb = 4,767; Kb = 1,71 x 10-5 при 20 ° С
pKb = 4.751; Kb = 1,774 х 10-5 при 25 ° С.
Повишаването на температурата почти незабележимо увеличава основността на амониевия хидроксид.
номенклатура
Какви са общите и официални имена, които NH получава?4ОН? Според установеното от IUPAC, името му е амониев хидроксид, защото съдържа хидроксил анион.
Амонякът по своя товар +1 е моновалентен, поради използването на номенклатурата като запас: амониев хидроксид (I).
Въпреки че използването на термина амониев хидроксид е технически неправилно, тъй като съединението не може да се изолира (поне не на Земята, както е обяснено подробно в първия раздел).
Освен това амониевият хидроксид получава наименованията на амонячна вода и течен амоняк.
разтворимост
NH4ОН, тъй като няма никаква сол в земни условия, не може да се прецени колко разтворим е в различни разтворители.
Може обаче да се очаква, че той е изключително разтворим във вода, тъй като разтварянето му ще освободи огромни количества NH3. Теоретично, това би било удивителен начин за съхранение и транспорт на амоняк.
В други разтворители, способни да приемат водородни връзки, като алкохоли и амини, може да се очаква, че също ще бъде много разтворим в тях. Тук NH катион4+ е донор на водородни мостове и OH- работи като и двете.
Примери за тези взаимодействия с метанол са: Н3N+-Н-OHCH3 и HO- - HOCH3 (OHCH3 показва, че кислородът получава водородната връзка, а не че метиловата група е свързана с Н).
рискове
-При контакт с очите причинява дразнене, което може да доведе до увреждане на очите.
-Той е корозивен. Следователно, при контакт с кожата може да предизвика дразнене и при високи концентрации на реагента, да причини изгаряния на кожата. Многократният контакт на амониевия хидроксид с кожата може да причини сухота, сърбеж и зачервяване (дерматит).
-Вдишването на спрей от амониев хидроксид може да предизвика остро възпаление на дихателните пътища, характеризиращо се с задушаване, кашлица или недостиг на въздух. Продължителното или многократно излагане на веществото може да доведе до повтарящи се бронхиални инфекции. Също така, вдишването на амониев хидроксид може да предизвика дразнене на белите дробове.
-Излагането на високи концентрации на амониев хидроксид може да бъде спешна медицинска помощ, тъй като може да настъпи натрупване на течности в белите дробове (белодробен оток)..
-Концентрацията от 25 ppm е взета като граница на експозиция, в 8-часово работно време, в среда, в която работникът е изложен на вредното действие на амониевия хидроксид.
реактивност
-Освен това, от потенциалната опасност за здравето от излагане на амониев хидроксид, има други предпазни мерки, които трябва да бъдат взети предвид при работа с веществото.
-Амониевият хидроксид може да реагира с много метали, като например сребро, мед, олово и цинк. Също така реагира със солите на тези метали, за да образуват експлозивни съединения и да освобождават водороден газ; което от своя страна е запалимо и експлозивно.
-Той може да реагира бурно със силни киселини, например: солна киселина, сярна киселина и азотна киселина. По същия начин, той реагира по същия начин с диметил сулфат и халогени.
-Реагира със силни основи, като натриев хидроксид и калиев хидроксид, произвеждащи газообразен амоняк. Това може да бъде проверено, ако се наблюдава равновесието в разтвора, в който се добавя ОН-йони- премества баланса до образуването на NH3.
-Мед и алуминиеви метали, както и други поцинковани метали, не трябва да се използват при работа с амониев хидроксид, поради неговото корозионно действие върху тях..
приложения
В храната
-Използва се като добавка в много храни, в които действа като раздробяващ агент, контрола на рН и довършител на повърхността на храната..
-Списъкът на храни, в които се използва амониев хидроксид, е обширен и включва печени изделия, сирена, шоколади, бонбони и пудинги.
-Амониевият хидроксид се класифицира като безопасно вещество от FDA за преработката на храни, при условие че се спазват установените стандарти.
-В месните продукти се използва като антимикробно средство, което е в състояние да елиминира бактерии, като например Е. coli, като я намалява до неоткриваеми нива. Бактериите се намират в червата на говедата, адаптирайки се към киселата среда. Амониевият хидроксид, чрез регулиране на рН, пречи на растежа на бактериите.
терапевтичен
-Амониевият хидроксид има няколко терапевтични приложения, включително:
-10% разтвор се използва като респираторен рефлексен стимулант
-Външно се използва върху кожата за лечение на ухапвания и ухапвания от насекоми. Действа върху храносмилателната система като антиацидно и газоносно, т.е..
В допълнение, той се използва като локално средство за остра и хронична мускулно-скелетна болка. Вследствие на руберационното действие на амониевия хидроксид се наблюдава локално повишаване на кръвния поток, зачервяване и дразнене..
Промишлени и разни
-Той действа в намаляването на NOx (високореактивни газове като азотен оксид (NO) и азотен диоксид (NO.)2)) за емисии от комина и намаляване на NOx в емисиите на комини.
-Използва се като пластифициращ агент; Добавка на бои и за обработка на повърхности.
-Той увеличава порьозността на косата, като позволява на пигментите на петна да имат по-голямо проникване, което постига по-добро завършване.
-Амониевият хидроксид се използва като антимикробно средство при третирането на отпадъчни води. В допълнение, той се намесва в синтеза на хлорамин. Това вещество изпълнява функция, подобна на хлора при пречистването на вода за плувни басейни, която има предимството да бъде по-малко токсична.
-Използва се като инхибитор на корозията в процеса на рафиниране на петрол.
-Използва се като почистващ препарат в различни промишлени и търговски продукти, използва се на няколко повърхности, включително: неръждаема стомана, порцелан, стъкло и фурна.
-Освен това, той се използва в производството на перилни препарати, сапуни, фармацевтични продукти и мастила.
В селското стопанство
Въпреки че не се прилага директно като тор, амониевият хидроксид изпълнява тази функция. Амонякът се произвежда от атмосферен азот по метода на Хабер-Бош и се транспортира в хладилник под точката на кипене (-33 ° С) до местата на неговото използване..
Амонякът под налягане се инжектира в парна форма в почвата, където веднага реагира с едафичната вода и преминава в амониева форма (NH)4+), който се задържа в местата за обмен на катиони. Освен това се получава амониев хидроксид. Тези съединения са източник на азот.
Заедно с фосфор и калий, азотът представлява триадата на основните хранителни вещества на растенията, които са от съществено значение за неговия растеж.
препратки
- Ganong, W. F. (2002) Медицинска физиология. 19-то издание. Редакционно Модерно Ръководство.
- A. D. Fortes, J.P. Brodholt, I. G. Wood и L. Vocadlo. (2001 г.). Ab initio симулация на амонячен монохидрат (NH3Н2О) и амониев хидроксид (NH4OH). Американски физически институт. J. Chem., Phys., Том 115, No. 15, 15.
- Helmenstine, Anne Marie, Ph.D. (6 февруари 2017 г.). Факти за амониев хидроксид. Изтеглено от: thoughtco.com
- Група Pochteca. (2015). Амониев хидроксид. pochteca.com.mx
- NJ Здраве (Н.О.). Информационен лист за опасни вещества: амониев хидроксид. [PDF]. Взето от: nj.gov
- Ученик по химия. (2018). Амониев хидроксид. Изтеглено от: chemistrylearner.com
- PubChem. (2018). Амониев хидроксид. Възстановен от: pubchem.ncbi.nlm.nih.gov


