Формула, свойства, рискове и приложения на литиевия оксид
на литиев оксид е неорганично химично съединение с формула Li2Или се образува заедно с малки количества литиев пероксид, когато литиевият метал се изгаря във въздуха и се комбинира с кислород..
До 1990-те години пазарът на метали и литий беше доминиран от американското производство от находища на минерали, но в началото на 21-ви век по-голямата част от производството беше получена от източници извън САЩ; Австралия, Чили и Португалия бяха най-важните доставчици в света. Боливия има половината от литиевите находища в света, но не е голям производител.
Най-важната търговска форма е литиев карбонат, Li2CO3, произведени от минерали или саламури чрез различни процеси.
Когато литий се изгаря във въздуха, основният продукт е бял оксид на литиев оксид, Li2О. В допълнение, произвежда се литиев пероксид, Li2О2, също бял.
Това може да се осъществи и чрез термично разлагане на литиев хидроксид, LiOH или литиев пероксид, Li2O2
4Li (s) + O2(g) → 2Li2O (s)
2LiOH (s) + топлина → Li2О (s) + Н2O (g)
2Li2О2(s) + топлина → 2Li2O (s) + O2(G)
Физични и химични свойства
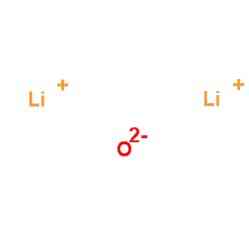
Литиев оксид е бяло твърдо вещество, известно като лития, което няма аромат и солен вкус. Външният му вид е показан на фигура 2 (Национален център за биотехнологична информация, 2017).

Фигура 2: външен вид на литиев оксид
Литиев оксид са кристали с геометрия на антифлорит, подобна на тази на натриев хлорид (кубичен центриран по лицата). Неговата кристална структура е представена на Фигура 3 (Марк Зима [Университетът на Шефийлд и WebElements Ltd, 2016].
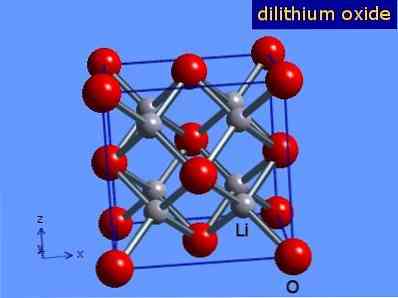
Фигура 3: кристална структура на литиев оксид.
Молекулното му тегло е 29,88 g / mol, плътността му е 2,013 g / ml, а точките на топене и кипене са съответно 1438 ° C и 2066 ° C. Съединението е много разтворимо във вода, алкохол, етер, пиридин и нитробензен (Royal Society of Chemistry, 2015).
Литиевият оксид реагира лесно с водна пара за образуване на хидроксид, а с въглероден диоксид за образуване на карбонат; следователно, той трябва да се съхранява и обработва в чиста и суха атмосфера.
Оксидните съединения не водят до електричество. Въпреки това, някои структурирани пероскитни оксиди са електронни проводими, които намират приложение в катода на твърди оксидни горивни клетки и системи за производство на кислород.
Те са съединения, които съдържат поне един кислороден анион и един метален катион (American Elements, S.F.).
Реактивност и опасности
Литиев оксид е стабилно съединение, несъвместимо със силни киселини, вода и въглероден диоксид. Доколкото ни е известно, химичните, физичните и токсикологичните свойства на литиев оксид не са изследвани и докладвани в дълбочина.
Токсичността на литиеви съединения е функция от тяхната разтворимост във вода. Литиевият йон има токсичност на централната нервна система. Съставът е силно корозивен дразнещ, ако влезе в контакт с очите, кожата, при вдишване или поглъщане (ESPI METALS, 1993).
В случай на контакт с очите трябва да проверите дали носите контактни лещи и да ги отстраните незабавно. Очите трябва да се изплакнат с течаща вода в продължение на най-малко 15 минути, като държите клепачите отворени. Можете да използвате студена вода. Мазта не трябва да се използва за очите.
Ако химикалът влезе в контакт с дрехите, отстранете го възможно най-бързо, като предпазите собствените си ръце и тяло. Поставете жертвата под предпазен душ.
Ако химичното вещество се натрупва върху откритата кожа на жертвата, като ръцете, внимателно и внимателно измийте кожата, замърсена с течаща вода и неабразивен сапун. Можете да използвате студена вода. Ако дразненето продължи, потърсете лекарска помощ. Измийте замърсеното облекло преди повторна употреба.
В случай на вдишване, на пострадалия трябва да се позволи да почива в добре проветрено помещение. Ако инхалацията е тежка, жертвата трябва да бъде евакуирана в безопасна зона възможно най-скоро.
Разхлабете плътно облекло, като якичка за риза, колани или вратовръзка. Ако на жертвата е трудно да диша, трябва да се приложи кислород. Ако жертвата не диша, се извършва реанимация от уста в уста.
Винаги, като се има предвид, че може да е опасно за лицето, което оказва помощ, за да се направи реанимация от устата в уста, когато вдишаният материал е токсичен, инфекциозен или корозивен.
Във всички случаи трябва незабавно да потърсите лекарска помощ (SIGMA-ALDRICH, 2010).
приложения
Литиевият оксид се използва като флюс в керамичните глазури и създава синьо с мед и рози с кобалт. Литиевият оксид реагира с вода и пара, образувайки литиев хидроксид и трябва да бъде изолиран от тях.
Литиев оксид (Li2О) с висок потенциал на тритий е привлекателен кандидат за твърдия културен материал на електроцентрала за синтез на DT, поради високата му плътност на литиеви атоми (в сравнение с други литиеви или метални литиеви керамики) и неговата проводимост относително висока топлина (LITHIUM OXIDE (Li2O), SF).
Ли2Или ще бъде изложена на високи температури при неутронно облъчване по време на работа на термоядрени одеяла. При тези обстоятелства в Li ще настъпи голям брой дефекти на облъчване2Или като например индуцирано с хелий набъбване, относително високо термично разширение, растеж на зърната, образуване на LiOH (T) и утаяване при ниски температури и транспортиране на LiOH (T) маса при високи температури.
В допълнение, Li2Или ще бъде подложен на напрежения, произтичащи от разлики в топлинното разширение между Li2О и структурни материали. Тези характеристики на Li2Или водят до предизвикателни инженерни проблеми както в производството, така и в дизайна на одеялото.
Възможна нова употреба като заместител на кобалт и литиев оксид като катод в литиево-йонни батерии, използвани за захранване на електронни устройства от мобилни телефони до лаптопи, както и за автомобили с батерии (Reade International Corp, 2016).
препратки
- Марк Уинтър [Университетът в Шефилд и WebElements Ltd. (2016). webelements. Взето от литий: дилитиев оксид webelements.com.
- Американски елементи. (S.F.). Литиев оксид. Взети от americanelements americanelements.com.
- ESPI МЕТАЛИ. (1993, юни). Литиев оксид. Взети от espimetals espimetals.com.
- Литиев оксид (Li2O). (S.F.). Взето от ferp.ucsd.edu ferp.ucsd.edu.
- Национален център за биотехнологична информация. (2017, 24 юни). PubChem Compound Database; CID = 166630. Взето от PubChem pubchem.ncbi.nlm.nih.gov.
- Reade International Corp. (2016). Прах от литиев оксид (Li2O). Взети от reade reade.com
- Кралско химическо дружество. (2015). Литиев оксид.Взето от chemspiderchemspider.com.
- Sigma-Aldrich. (2010). Информационен лист за безопасност Литиев оксид. Взето от chemblink chemblink.com.


