Основа, материали, техника и приложения за оцветяване по грам
на Грам оцветяване е най-простата и полезна техника за оцветяване в диагностичната микробиология. Тази техника е създадена от датския лекар Ханс Кристиан Грам през 1884 г., който успява да класифицира бактериите в грам-положителни и грамотрицателни, според състава на клетъчната стена..
Техниката претърпява някои модификации от Хъкър през 1921 г., за да стабилизира реагентите и да подобри качеството на оцветяването, така че оцветяването по Грам е известно и като Грам-Хъкър..
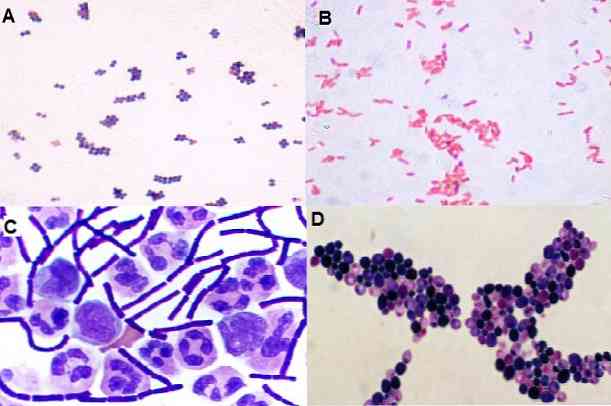
С тази техника е възможно да се наблюдава и формата, която имат микроорганизмите, т.е. дали те са коки, бацили, кокобацили, плеоморфни, нишковидни, наред с други. Както и разпределението му в пространството: в клъстер, във верига, изолирано, по двойки, в тетради и др..
Когато се подозира бактериална инфекция, повечето от получените проби трябва да се разпределят върху предметно стъкло и да се оцветят с грам за изследване под микроскоп..
Докладът на Грам ще ръководи лекаря какъв тип микроорганизъм може да бъде причината за инфекцията, преди да получи крайния резултат на културата.
В някои случаи животът на пациента е много компрометиран, така че лекарите спешно се нуждаят от доклада Грам, за да направят емпирично лечение, докато чакат за идентифициране на микроорганизма..
Например, ако Грам покаже, че има Грам положителни коки в цереброспиналната течност, лекарят ще ориентира първоначалната терапия с антибиотици, които елиминират този тип бактерии, съгласно установените за него протоколи..
След като пристигне крайният резултат с името на изолирания микроорганизъм и съответния му антибиограма, лекарят ще прецени дали да промени терапията. Това решение ще бъде взето в съответствие с проучването на чувствителността на микроорганизма към антибиотиците, които той получава и еволюцията на пациента..
индекс
- 1 Фондация
- 2 Материали
- 3 Приготвяне на багрила и реактиви
- 3.1 Разтвор на кристално виолетово
- 3.2 Йодо-Лугол
- 3.3 Избелване
- 3.4 Контраст
- 4 Съхранение на реактиви
- 5 Приготвяне на разпространението на пробата за оцветяване
- 5.1-Gram директни проби
- 5.2-Грам от култури
- 6 Техника
- 7 Помощна програма
- 8 Чести грешки
- 9 Препратки
фундамент
Това е техника, която представя 4 фундаментални стъпки: оцветяване, фиксация с разяждащото вещество, обезцветяване и контрактация. Ето защо, тази техника в допълнение към оцветяването на бактериите, също ги отличава.
Кристалната виолетка е първият използван оцветител. Той има афинитет към пептидогликан и лилаво ще оцветява всички присъстващи бактерии, след това се поставя луголът, който действа като разхлабител, т.е..
Грам-положителните бактерии, които имат дебела стена на пептидогликан, образуват повече комплекси (кристален виолет-йод), затова запазват багрилото..
Той също така влияе, че грам-положителните стени на бактериите съдържат по-голямо количество ненаситени киселини, които показват висок афинитет към окислители (Lugol).
Междувременно Грам-отрицателните бактерии имат тънък слой пептидогликан, което прави бактериите по-сложни от Грам-положителните бактерии..
След това идва стъпката на обезцветяване, където Грам положителни и Грам отрицателни бактерии се държат различно.
Грам отрицателните бактерии съдържат външна мембрана, богата на липополизахариди, която е част от нейната клетъчна стена. Мазнините се разрушават при контакт с алкохол ацетон, така че външната мембрана се дестабилизира, като виолетовият кристал се освобождава.
Така се оцветява със сафранин или основен фуксин, като се получава червен цвят.
В случай на грам-положителни бактерии, те устояват на обезцветяване, защото белина действа за затваряне на порите, което предотвратява излизането на кристално-виолетовия / йодния комплекс.
Следователно, оцветяването с виолетовия кристал е стабилно и няма място за сафранин или фуксин. Поради това, тези бактерии петна интензивно синьо или лилаво.
материали
Комплектът за оцветяване на Gram се състои от:
- Виолетов кристал
- Лугол
- Ацетон алкохол
- Сафранин или основен фуксин
Приготвяне на багрила и реактиви
Разтвор на кристално виолетово
Решение А:
Виолетов кристал -2 гр
Етилов алкохол 95% -20cc
Решение Б:
Амониев оксалат -0.8 гр
Дестилирана вода-80 cc
За окончателното приготвяне на виолетовия кристал, разтворът 1:10 трябва да се разреди с дестилирана вода и да се смеси с 4 части разтвор Б. Сместа се съхранява 24 часа преди употреба. Филтрира се в колба за оцветяване с кехлибар, като се използва хартиен филтър.
Количеството, което ще се използва ежедневно, се прехвърля в кехлибарена бутилка с капкомер.
Йод-Лугол
Претеглете и измерете посоченото количество от всяко съединение, както следва:
Кристали на Йодо - 1гр
Калиев йодид - 2гр
Дестилирана вода -300 cc
Калиевият йодид се разтваря малко по малко във водата и след това се добавя йод. Разтворът се обръсва до кехлибарена бутилка.
Количеството, което ще се използва ежедневно, се прехвърля в по-малка кехлибарена бутилка с капкомер.
избелване
95% етилов алкохол -50 ml
Ацетон - 50 ml
Подготвя се на равни части. Покрийте я добре, има тенденция да се изпарява.
Поставете в бутилка с капкомер.
Този препарат осигурява обезцветяване в умерено време 5-10 секунди и е най-препоръчителното.
Начинаещите предпочитат да използват само 95% етилов алкохол, където обезцветяването е по-бавно от 10 до 30 сек.
Докато най-опитните могат да използват чист ацетон, където обезцветяването става много бързо от 1 до 5 секунди.
контраст
Основен разтвор на сафранин
Сафранина -2.5 гр
Етилов алкохол 95% -100 cc
След претегляне посоченото количество сафранин се разтваря в 100 см3 етилов алкохол до 95%.
Работният разтвор на сафранин се приготвя от основния разтвор.
За да направите това, измерете 10 см3 от основния разтвор, добавете 90 см3 дестилирана вода, за да завършите 100 мл.
Препоръчително е да прехвърлите сумата, която ще се използва ежедневно, в кехлибарена бутилка с капкомер.
Микроорганизми, които оцветяват слабо грам-отрицателни с Gram-Hucker оцветяване, като някои анаероби \ t, Legionella sp, Campylobacter sp и Brucella sp, те могат да бъдат много по-добре оцветени, ако се използва модификацията, направена от Kopeloff до Gram-Hucker оцветяване, наречена Gram-Kopeloff оцветяване, се използва.
Тази техника променя боята на сафранин с основен фуксин. С тази модификация е възможно ефективно да се оцветят гореспоменатите микроорганизми.
Съхранение на реактиви
Готовите багрила трябва да се съхраняват при стайна температура.
Приготвянето на пробата се разпространява в цвят
Пробата трябва да съдържа поне 105 микроорганизми преди наблюдение на микроорганизма в намазка е вероятно. Спредовете могат да бъдат направени от директна проба или култури в твърда или течна среда.
Спредовете трябва да бъдат еднакви, добре разпределени и не твърде дебели, за по-добра визуализация на наличните структури.
-Грам от директни проби
Уринен грам без центрофуга
Урината се смесва и 10 μl се поставя върху предметно стъкло. Наблюдението на поне едно бактериално / потапящо поле показва, че има инфекция.
Това означава, че културата ще има приблизително повече от 100,000 CFU / ml (105 CFU / mL) на урината в 85% от случаите.
Този метод не е полезен за броя на колониите под 100,000 CFU.
LCR Gram
CSF трябва да се центрофугира, супернатантата да се отстрани и пелетата да се разпространи върху предметно стъкло. Тази течност е стерилна при нормални условия; наблюдението на бактериите показва инфекция.
Грам от респираторни проби
Грам, бронхиален или бронхоалвеоларен лаваж, въпреки че може да има различни микроорганизми, винаги ще ви помагат при диагностицирането, освен че са полезни и вида на наблюдаваните клетки..
В случай на храчки, намазката трябва да се приготви с най-гнойните части от пробата.
Табуретка Грам
Не се препоръчва извършването на грам за този тип проби, тъй като няма диагностична стойност.
-Грам
Те могат да се правят по два начина: един от течни култури и друг от твърди култури.
Течни култури
От течни култури е изключително проста; под запалката се вземат няколко изпичания от мътния бульон и те се поставят на чист и сух слайд, давайки кръгови движения от центъра към периферията, за да разпределят материала равномерно.
Оставя се да изсъхне спонтанно във въздуха. Веднъж изсъхнал, материалът се фиксира към листа с топлина. За целта, с помощта на скоба, листът 3 преминава 4 пъти през пламъка на горелката Bunsen, като се внимава да не се изгори материалът.
Листът се оставя да се охлади и се поставя върху оцветяващия мост.
Твърди култури
За да извършите разширение за оцветяване с грам от твърда култура, продължете както следва:
Преди да се изберат колониите, които трябва да се вземат, слайда трябва да се приготви, като се поставят приблизително две капки от стерилен физиологичен солев разтвор.
Ако оригиналната плоча на културата съдържа няколко различни типа колонии, ще бъде избрана изолирана колония от всяка една, за да се изпълни грам. Всяка колония ще бъде взета с платинената верига, за да се разтвори в солен разтвор, поставен преди това върху предметното стъкло.
Кръгови движения се дават от центъра към периферията, за да се разпредели хомогенно колонията върху слайда..
Оставя се да изсъхне спонтанно във въздуха. След като изсъхне, листът се фиксира с топлина, както е обяснено по-горе (пламък на плъзгача със запалката), като се внимава да не се изгори материал.
Тази процедура трябва да се извърши с всеки различен тип колония. На лист хартия трябва да се отбележи реда на наблюдаваното, например:
Колония 1: Жълта бета-хемолитична колония: Грам-положителни коки се наблюдават в клъстери
Колония 2: Кремообразна колония, без хемолиза: Наблюдавани са грам отрицателни коккобацили.
Всеки лист трябва да има етикет, за да знае какво наблюдаваме.
техниката
Техниката на оцветяване с грам е изключително лесна за изпълнение и сравнително евтина и не може да бъде пропусната в микробиологична лаборатория.
Същото се прави както следва:
- Фиксирайте намазката с топлина и поставете върху цветния мост.
- Листът е покрит изцяло с виолетово стъкло за 1 минута.
- Измийте с вода. Не изсушавайте
- Плаката се покрива с разтвор на Lugol, оставя се 1 минута. Измийте с вода. Не изсушавайте.
- Смесва се за 5-10 секунди с леко разбъркване в ацетонов алкохол. Или поставете листа в изправено положение и изпуснете капчиците от обезцветяващия агент на повърхността, докато останалото виолетово стъкло се изтегли. Не превишавайте.
- Измийте с вода. Не изсушавайте.
- Заместете листа върху цветния мост и покрийте за 30 секунди със сафранин (Gram-Hucker) или 1 минута с основен фуксин (Gram-Kopeloff).
- Измийте с вода
- Оставя се да изсъхне спонтанно във вертикален въздух.
След като изсъхне, поставете 1 капка потапящо масло, за да го наблюдавате под оптичния микроскоп под 100Х.
полезност
Тази техника позволява да се разграничат морфотипиантите от повечето бактерии.
Дрождите също се отличават с този цвят. Те вземат кристално-виолетовото, което означава, че оцветяват грам положително.
От друга страна, могат да се разграничат грам-положителни спори-формиращи бацили, в които се наблюдава ясно пространство във вътрешността на бацила, където се формира ендоспората, въпреки че спорите не се оцветяват добре. За да се използват спори, се използват други техники като Шефер-Фултон.
Трябва да се отбележи, че това оцветяване не служи за оцветяване на всички видове бактерии, т.е. има случаи, при които оцветяването не работи.
В този случай могат да се споменат бактерии, които нямат клетъчна стена. Например: род Mycoplasma, сферопласти, Ureaplasma, L-форми и протопласти.
Той също така петна силно бактерии със стени, богати на миколови киселини, като микобактерии и вътреклетъчни бактерии като Chlamydias и Rickettsias.
Също така е неефективно да се оцветят повечето спирохетални бактерии.
Има бактерии от същия род, които могат да бъдат наблюдавани в една и съща проба с грам положителни и като грам отрицателни. Когато това се случи, то се нарича променливо Грам оцветяване, което може да се дължи на промяна в хранителните вещества, температура, рН или концентрация на електролити..
Често срещани грешки
Избледнявайте прекалено
Преувеличаването в стъпката на обезцветяване може да предизвика наблюдение на фалшиви грам-отрицателни микроорганизми.
Не чакайте достатъчно време за сушене, за да добавите потапящото масло:
Тази грешка причинява образуването на мастни мицели, които затрудняват наблюдението на наличните структури. Това се случва, когато маслото се присъединява към водните молекули, присъстващи в размазването.
Обратно на реда на реагентите:
Една такава грешка ще накара Грам-отрицателните бактерии да показват лилаво, т.е. фалшиво Грам-положително.
Използвайте стари култури (твърди или течни):
Той може да причини грам-положителни бактерии да оцветят грамотрицателен (фалшив грам отрицателен). Това се случва, защото в старите култури е вероятно да има мъртви или влошени бактерии и при тези условия бактериите не запазват виолетовия кристал..
Използвайте много стар разтвор на Lugol:
С течение на времето луголът губи свойствата си и цвят избледнява. Ако се използва вече дегенерираният реагент, той няма да фиксира кристалната виолетова ямка, следователно съществува възможност за получаване на визуализация на микроорганизми, които са фалшиво грам отрицателни..
Синкав фон
Правилно обезцветеният фон ще бъде червен. Синият фон показва, че обезцветяването е недостатъчно.
препратки
- Ryan KJ, Ray C. 2010. Sherris. микробиология Медицински, 6-то издание McGraw-Hill, Ню Йорк, САЩ
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Микробиологична диагноза. (5-то изд.). Аржентина, редакция Panamericana S.A..
- Forbes B, Sahm D, Weissfeld A. 2009. Микробиологична диагноза на Bailey & Scott. 12 изд. Аржентина. Panamericana S.A Редакция
- Casas-Rincón G. 1994. Обща микология. Второ издание на Университета на Венецуела, Библиотечни издания. Венецуела, Каракас.
- "Грам байц" Уикипедия, Свободната енциклопедия. 4 октомври 2018 г., 23:40 UTC. 9 декември 2018, 17:11. Взето от es.wikipedia.org.
- González M, González N. 2011. Ръководство за медицинска микробиология. Второ издание, Венецуела: Дирекция на медиите и публикации на Университета в Карабобо.
- López-Jácome L, Hernández-Durán M, Colín-Castro C, Ortega-Peña S, Cerón-González G, Franco-Cendejas F. Основно оцветяване в микробиологичната лаборатория. Проучване на уврежданията. 2014; 3 (1): 10-18.


