Натриев бензоат структура, свойства, синтез, употреби и рискове
на натриев бензоат е органична сол, чиято химична формула е С6Н5COONa. Той се произвежда или генерира чрез реакция на неутрализация между бензоена киселина и натриев хидроксид. Резултатът е бяло твърдо вещество (дъно), разтворимо във вода и се разлага чрез нагряване при 120 ° С.
Тази сол може да бъде намерена естествено в различни плодове и други части на зеленчуци, като: боровинки, сливи, стафиди, канела, карамфил и ябълки. Той е и метаболит на водорасли и растения.

Натриевият бензоат не се натрупва в тялото, тъй като бързо се съчетава с аминокиселината глицин, за да образува хипурова киселина, която се отделя свободно с урината..
Това съединение се използва с консервант за храни, неговото действие е по-ефективно при кисело рН. Това се дължи на присъствието на органични киселини, които придават на храната рН, подходящ за действието на натриев бензоат; който като такъв завършва с протониран до бензоена киселина.
Тази сол се използва и при лечението на наследствени метаболитни нарушения на цикъла на урея, което произвежда натрупването на междинен метаболит, за който ензимът, който обработва, е недостатъчен..
Международната програма за химическа безопасност не открива вредни ефекти на натриев бензоат върху хората при консумация между 647 - 825 mg / kg телесна маса..
Съобщава се обаче, че натриевият бензоат може да предизвика псевдо-алергични реакции и да обостри симптомите при пациенти с чести епизоди на уртикария и астма..
индекс
- 1 Структура на натриев бензоат
- 2 Свойства
- 2.1 Химични наименования
- 2.2 Физическо описание
- 2.3 Миризма
- 2.4 Вкус
- 2.5 Точка на запалване
- 2.6 Автоматично запалване
- 2.7 Плътност
- 2.8 Разтворимост
- 2.9 Стабилност
- 2.10 Разлагане
- 2.11 рН
- 2.12 Повърхностно напрежение
- 3 Резюме
- 4 Използване
- 4.1 В храната
- 4.2 Медицинско лечение
- 4.3 Други
- 5 Рискове
- 6 Препратки
Структура на натриев бензоат
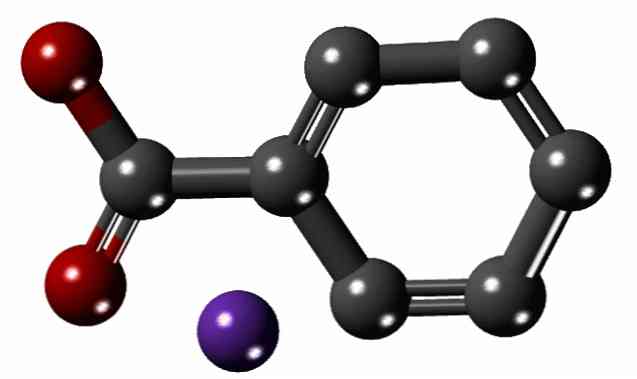
В горното изображение структурата на натриевия бензоат е показана с модел на сфери и пръти. Ароматният пръстен може да се види с просто око, с карбоксилатната група, -СОО-, свързана с нея (тази на червените сфери); последният, от своя страна, електростатично привлича Na катиона+ (пурпурна сфера).
Тъй като разликата в размерите между двата йона е голяма (сравни в изображението), не е изненадващо, че ретикуларната енергия на кристалите на натриевия бензоат е ниска. Това води до това, че техните кристали имат естествена склонност да разтварят в полярни разтворители или да претърпят серия от химични реакции.
C6Н5COO- Той може да приеме два водородни моста от две водни молекули, което благоприятства неговата хидратация. Междувременно Na+ Той също завършва разтворени с вода, преодолявайки електростатичните сили, които го задържат заедно със С6Н5COO-.
Така че, тази сол е съставена от С йони6Н5COO- и Na+, които са подредени по строг начин за изграждане на кристали. В литературата не е получена информация за неговата кристална структура, така че не е известно какъв е типът на единичната клетка за тази сол.
свойства
Химични наименования
-Натриев бензоат
-Натриева сол на бензоената киселина
-Sobenato
-Antimol.
Физическо описание
Бели гранули или кристален прах. Безцветен кристален прах.
миризма
тоалетна.
вкус
Горчиво, стягащо и неприятно.
Точка на запалване
> 100 ° С.
Автоматично запалване
> 500 ° С.
плътност
1.50 g / cm3.
разтворимост
-Разтворим в течен амоний и пиридин.
-Леко разтворим в етанол: 8.22 g / 100 g при 25 ° С.
-В метанол той е по-разтворим, отколкото в етанол: 8.22 g / 100 g при 15 ° С.
стабилност
Той е стабилен при препоръчаните условия на съхранение. Той може да бъде чувствителен към влага, хидролизира се до бензоена киселина. Несъвместимо със силни окислители, основи и минерални киселини.
разлагане
Когато се нагрява до разлагане при 120 ° C (248 ° F), той излъчва остър дим от натриев оксид и други компоненти, които могат да бъдат токсични и канцерогенни.
Когато се разлага при 120 ° C, се предотвратява точността на кипене и точка на топене, като докладваните стойности на тези параметри са теоретични..
рН
Близо до 8, разтворени във вода. Това е основна сол. Това е така, защото хидролизира до освобождаване на ОН-йони-.
Повърхностно напрежение
72,9 mN / cm при 20 ° С в разтвор от 1 g / l вода.
синтез
Бензоената киселина, участваща в синтеза на натриев бензоат, се произвежда основно по три метода:
-Нафталенът се окислява с ванадиев пентоксид, за да се образува фталов анхидрид. Това съединение може да претърпи декарбоксилиране, за да предизвика бензоена киселина, тъй като в неговата структура с два ароматни пръстена изглежда, че има две -COO групи, кондензирани заедно.
-Толуенът се окислява до бензоена киселина чрез добавяне на азотна киселина. В тази реакция метиловата група "просто" се окислява до карбоксилната група:
C6Н5СН3 => С6Н5COOH
-И накрая, бензотрихлоридът се хидролизира чрез действието на минерални киселини с произход от бензоена киселина.
Получава се бензоена киселина по някой от тези три метода, след което се разтваря в натриев хидроксид. Тези съединения претърпяват реакция на неутрализация, произвеждаща натриев бензоат и вода.
C6Н5СООН + NaOH => С6Н5COONa + H2О
Реакцията може също да се проведе с натриев карбонат, въпреки че неговият добив може да бъде по-малък от желания.
приложения
В храната
Натриевият бензоат е консервиращо средство за храна, което може да инхибира или забавя процеса на ферментация, подкисляването или всеки процес, който ги влошава. В допълнение, натриевият бензоат има фунгицидно действие.
Тази сол е в състояние да елиминира дрождите, бактериите и гъбите, присъстващи в храната. Неговото консервиращо действие е по-ефективно при рН < 6; es decir, en condiciones ácidas. Por esta razón es usado en conservas y en aliños de ensaladas que contienen vinagre (ácido acético).
Натриевият бензоат се използва и за съхранение на газирани напитки и безалкохолни напитки, в които присъства въглеродна киселина. Също и в конфитюри, богати на лимонена киселина и като цяло в храни с присъстващи киселини, които създават кисела среда.
В допълнение, той се използва във фуража с концентрация на натриев бензоат от 0.1%. Максималното количество бензоена киселина и натриев бензоат, използвани като консерванти в храната, не надвишава 2 000 mg / kg храна.
Медицинско лечение
Остра хиперамонемия
Натриевият фенилацетат и натриевият бензоат се използват под формата на адювантни терапии за лечение на остра хиперамонемия и свързана енцефалопатия при пациенти с промени в цикъла на урея..
Тези съединения са класифицирани като лекарства сираци. Това наименование се отнася за лекарства, които не са печеливши от икономическа гледна точка.
шизофрения
Натриев бензоат се използва експериментално при лечението на шизофрения. Централната част на изследването е ролята, която в лечението изпълнява инхибирането на ензимите на D-аминокиселините, активността, която отговаря на натриевия бензоат..
Аргиносукцинова киселина
Натриевият бензоат се използва при лечението на аргининосукцинова киселина, наследствено метаболитно нарушение, което може да причини на пациентите повишаване на концентрацията на амоний, способно да повлияе на централната нервна система..
задържащ
-Той е инхибитор на ензима araquidonato 15-липоксигеназа, ензим, който е изследван от фармацевтичната индустрия за участие в коронарна болест на сърцето.
-Той инхибира действието на липазния ензим триацилглицериди, ензим, който действа за освобождаване на глицерол и мастни киселини в тънките черва, като по този начин позволява абсорбцията на тези липиди, присъстващи в храната..
Възможно е да се използва натриев бензоат за регулиране на чревната абсорбция на липиди, като триацилглицериди..
Наследствени заболявания
Натриевият бензоат се използва за лечение на няколко наследствени заболявания, свързани с метаболизма на аминокиселините, сред които са споменати: лечение на хиперергининемия и лечение на дефицита на ензимната транслоказа на орнитин.
други
-Използва се при изплакване на алкохол и при полиране на сребро. В допълнение, той се използва при изработването на пиротехнически съединения, като е отговорен за свирката, която се произвежда, когато те се запалват.
-Използва се като антикорозионен, което е едно от основните изисквания при производството на тази сол. Използва се също в охлаждащи течности, антифриз и други системи на водна основа.
-При формулирането на пластмаси като полипропилен, той се използва за подобряване на неговата здравина и яснота.
-Служи като стабилизатор в баните и фотографски процеси.
рискове
Натриевият бензоат се класифицира от FDA като "обикновено безопасен", при доза от 0,1% от теглото на храната. Не се счита за дразнещ за контакт с кожата и очите, така че може да се каже, че острата токсичност е ниска.
Въпреки това, натриевият бензоат може да предизвика неимунологични реакции (псевдоалергия) чрез контакт. Този ефект е рядък при нормални хора, но при пациенти с чести епизоди на уртикария или симптоми на астма може да се наблюдава повишаване на честотата на тези симптоми..
При проучвания при плъхове и мишки не са открити данни за канцерогенно действие на натриев бензоат.
Беше посочено неудобството от използването му в присъствието на аскорбинова киселина, която може да произведе бензол; токсично съединение, посочено като канцерогенно.
препратки
- Net Industries. (2019). Производство на натриев бензоат. Изтеглено от: science.jrank.org
- Wikipedia. (2019). Натриев бензоат. Изтеглено от: en.wikipedia.org
- PubChem. (2019). Натриев бензоат. Изтеглено от: pubchem.ncbi.nim.nih.gov
- Hanes T. (2019). Факти за натриев бензоат. Livestrong. Изтеглено от: livestrong.com
- Химическа книга. (2017). Натриев бензоат. Изтеглено от: chemicalbook.com
- Lane H. et al. (2013) Джама психиатрия. 70 (12): 1267-1275.
- Световна здравна организация Женева. (12 април 2005 г.). Бензоена киселина и натриев бензоат. [PDF]. Изтеглено от: who.int


