Формула на калциев хидроксид, свойства, реактивност и употреба
на калциев хидроксид, известен също като хидратна вар или гасена вар, е неорганично съединение с формула Ca (OH)2.
Калциевият хидроксид приема полимерна структура, подобно на всички метални хидроксиди, като е идентична с тази на магнезиев хидроксид (Mg (OH))2) също известен като brucita.
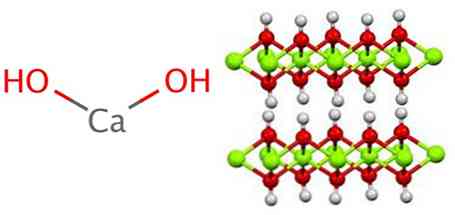
Вижда се, че в тази структура има образуване на водородни мостове. Калциевият хидроксид се синтезира индустриално чрез взаимодействие на калциев оксид, известен също като вар или негасена вар, с вода съгласно следната реакция:
CaOH + H2O → Ca (OH)2
Също така се приготвя в лабораторията чрез реакция между воден калциев хлорид и натриев хидроксид.
Калциевият хидроксид се среща естествено, но рядко в минералната си форма като портландит, който се среща в някои вулканични и метаморфни скали. (Формула на калциев хидроксид - използване, свойства, структура и формула на калциев хидроксид, 2005-2017).
Това съединение е широко разпространено и в циментови, разтворителни и промишлени почистващи препарати (като строителни продукти), за почистване на подове, за почистване на тухли, за продукти за уплътняване на цимент и много други..
Водният разтвор обикновено се нарича варовик. Варовичната вода се приготвя чрез разбъркване на калциев хидроксид в чиста вода и филтриране на излишъка от Са (ОН).2 не се разтваря.
Когато към варната вода се добави излишък от калциев хидроксид, се получава суспензия от частици калциев хидроксид, която й придава млечен вид, като в този случай има общо наименование на варовото мляко. Млякото от вар или наситен разтвор на вар (вар с вода) има рН 12,3, което е от основно естество.
Физични и химични свойства на калциев хидроксид
Калциев хидроксид е бял или безцветен прах, без миризма. Във воден разтвор (наситени разтвори) той има млечен вид поради супернатанта на неразтворен калциев хидроксид.
Ненаситените разтвори обикновено са бистри и безцветни разтвори, с лек земен мирис и горчив алкален вкус на калциев хидроксид. Появата на съединението е илюстрирана на Фигура 3 (Royal Society of Chemistry, 2015).

Калциевият хидроксид има молекулно тегло 74.093 g / mol и плътност 2.211 g / стз в твърдо състояние. Точката на топене е 580 градуса. Тя е слабо разтворима във вода, като може да разтвори 1,89 грама на литър при 0 ° C, 1,73 грама на литър при 20 ° C и 0,66 грама на литър при 100 ° C..
Разтворим е в глицерол и в кисели разтвори. Той е неразтворим в алкохол (Национален център за биотехнологична информация, S.F.).
Калциевият хидроксид е частично разтворен във вода, за да се получи разтвор, наречен варовик, който е умерена база. Водна вар или Ca (OH)2 (aq) Той реагира с киселини за образуване на соли и може да атакува някои метали като алуминий. Калциевата вода реагира лесно с въглероден диоксид, за да образува калциев карбонат, полезен процес, наречен карбонизация:
Ca (OH)2 + CO2 → CaCO3 + Н2О
Нитропарафини, нитрометан, нитропропан и т.н. образуват соли с неорганични основи като калциев хидроксид. Тези сухи соли са експлозивни. Съединението е химически подобно на натриев хидроксид (NaOH) или натриев оксид (Na2О). Те неутрализират киселините екзотермично, за да образуват соли плюс вода.
Смесването на тези материали с вода може да генерира опасни количества топлина, тъй като основата се разтваря или разрежда. Базите реагират с определени метали (като алуминий и цинк), за да образуват метални оксиди или хидроксиди и генерират водороден газ.
Базите могат да инициират реакции на полимеризация в полимеризиращи се органични съединения, особено епоксиди. Запалими и / или токсични газове могат да бъдат генерирани с амониеви соли, нитриди, халогенирани органични вещества, различни метали, пероксиди и хидропероксиди. Този тип съединение често служи като катализатор (Химически информационен лист CALCIUM HYDROXIDE, S.F.).
Реактивност и опасности

Калциев хидроксид е стабилно съединение, въпреки че е несъвместимо със силни киселини. Той е класифициран като дразнещо съединение и сред неговите опасности можем да подчертаем:
Той е корозивен за очите (причинява увреждане на роговицата или слепота) и кожата (произвежда възпаление и мехури).
Вдишването на прах ще предизвика дразнене в стомашно-чревния или дихателния тракт, характеризиращо се с изгаряне, кихане и кашлица. Тежкото преекспониране може да причини увреждане на белите дробове, асфиксия, безсъзнание или смърт. Възпалението на окото се характеризира с зачервяване, дразнене и сърбеж (Информационен лист за безопасност на калциев хидроксид, 2013).
Многократното излагане на очите при ниско ниво на прах може да предизвика дразнене и локално разрушаване на кожата или дерматит на кожата. Многократното вдишване на прах може да доведе до различна степен на дразнене на дихателните пътища или увреждане на белите дробове.
Ако този химикал влезе в контакт с очите, те трябва да се измият незабавно с големи количества вода, като от време на време повдигнете долните и горните клепачи. Трябва да се получи незабавна медицинска помощ. Контактните лещи не трябва да се използват при работа с този химикал.
Ако този химикал влезе в контакт с кожата, кожата, замърсена със сапун и вода, трябва незабавно да се изплакне. Ако този химикал проникне в дрехите, незабавно отстранете дрехите и изплакнете кожата с вода. Ако дразненето продължи след измиване, потърсете медицинска помощ.
Ако се вдишат големи количества от този химикал, изложеното лице трябва незабавно да се премести на чист въздух. Ако дишането е спряло, извършвайте реанимация от устата в уста, като същевременно запазвате жертвата на топло и в покой. Потърсете медицинска помощ възможно най-скоро.
При поглъщане незабавно да се потърси медицинска помощ и, ако е възможно, да се покаже контейнер или етикет (отравяне с калциев хидроксид, 2017 г.).
Работа и съхранение
- Съединението трябва да се съхранява в сух контейнер.
- Не поглъщайте или вдишвайте праха.
- Вода никога не трябва да се добавя към този продукт.
- В случай на липса на вентилация, вземете подходящо оборудване за дишане.
- Избягвайте контакт с кожата и очите.
- Пазете от несъвместими като киселини.
- Съхранявайте контейнера плътно затворен.
- Съхранявайте контейнера на хладно и добре проветриво място. Да не се съхранява над 25 градуса по Целзий.
Употреби и приложения

Калциевият хидроксид се произвежда в голям мащаб, лесно се обработва и обикновено е евтин, затова има много забележителни приложения и приложения.
Значително приложение на калциев хидроксид е като флокулант във водата и пречистването на отпадъчни води. Образува пухкаво заредено твърдо вещество, което помага за отстраняването на по-малки частици от водата, което води до по-лек продукт.
Това приложение се осигурява от ниската цена и ниската токсичност на калциевия хидроксид. Използва се също за пречистване на прясна вода, за да се повиши рН на водата. Целта е тръбите да не корозират, когато основната вода е кисела.
Друго голямо приложение е в хартиената промишленост, където се използва в производството на натриев хидроксид. Това превръщане е компонент на известния крафт процес, който се използва при екстракцията на пулпа.
В системи за поддържане на живота като скрубер с въглероден диоксид, по-специално в респиратори за гмуркане със затворена верига, където литиевият хидроксид, който е по-каустик, се счита за твърде рискован.
Използва се като съставка при избелването и мазилката, с така наречените варови разтвори. При пътното строителство калциевият хидроксид служи за подобряване на качеството на почвата.
Според Националния институт по здравеопазването, калциевият хидроксид обикновено се използва в стоматологичната дейност като антимикробно средство и е предпочитано вещество за образуване на защитен слой, известен като апикална бариера..
Апикалните бариери обикновено се използват като средство за избягване на некроза на пулпата в ситуации, при които ендодонтската хирургия е особено трудна, което обикновено е резултат от незрял постоянен зъб..
Тъй като калциевият хидроксид може да помогне за дезинфекция на зъб, когато вече съществува инфекция, той може да се използва като краткотрайно лечение за намаляване на болката и възпалението при подготовката за ендодонтска хирургия (Gottfried Schmalz, 2009).
Той служи като добавка за морската вода, тъй като намалява атмосферния CO2 и намалява парниковия ефект.
При производството на метали, варовикът се инжектира в потока отпадъчни газове, за да неутрализира киселини, като флуориди и хлориди, преди да бъдат изпуснати в атмосферата..
Калциев хидроксид се използва като активна алкална съставка в някои продукти за релаксация на косата.
Според Центъра за изследвания на материалите на Корнел, калциевият хидроксид може да изправи къдрава коса, защото разрушава дисулфидните връзки, които свързват цистеините, аминокиселините, които присъстват в по-високи концентрации в естествено къдрава коса. Разрушаването на тези връзки и запечатването им с калциев хидроксид постоянно променя физическата структура на третираната коса.
В бордоската смес калциевият хидроксид служи за неутрализиране на разтвора и образуване на дълготраен фунгицид.
Използва се в нефтопреработвателната промишленост за производството на петролни добавки (салицилати, сулфиди, феноли), в нефтохимическата промишленост за производство на твърди масла от различни марки, както и в химическата промишленост за производство на калциев стеарат. , Той обикновено се използва за изследване на абсорбцията на въглероден диоксид и газ.
Калциев хидроксид се използва при производството на спирачни накладки, при подготовката на сухи смеси за боядисване и декориране, а също и в производството на смеси за пестициди.
Използва се също като калциева добавка и рН / карбонатен буфер за аквакултурата на коралите в рифовите аквариуми.
Това е "алтернативен" естествен инсектицид, повечето от пълзящите насекоми, умират от контакт с него, включително кърлежи, бълхи, бръмбари и ларви (Russiver, 2015).
Калциевият хидроксид е ефективно решение за отделяне на косата от кожата на животните при подготовката му за производство на кожа.
Смес от калциев хидроксид и топла вода създава вана, в която пресните кожи трябва да се напоят до четири дни и да се разклащат често. Този процес разхлабва косата и кожата до такава степен, че обикновено може да се отстрани ръчно.
Поради ниската си токсичност и мекотата на основните си свойства, гасената вар се използва широко в хранителната промишленост за:
- Да се изясни суровият сок от захарна тръстика или захарно цвекло в захарната промишленост, пречиствателната вода за алкохолни напитки и безалкохолни напитки, кисели краставички и други храни.
- Направете царевични питки (помогнете на царевичното брашно да се съберат заедно). Зърната, варени с вар, се превръщат в никстамал, което значително увеличава бионаличността на ниацин, също се счита за по-вкусно и по-лесно за храносмилане..
- Почистете саламурата на калциевите и магнезиевите карбонати при производството на сол за хранителна и фармацевтична употреба.
- Подсилени плодови напитки, като портокалов сок и формула за кърмачета (BAUM, 2013).
препратки
- BAUM, J. (2013, 16 август). Използване на калциев хидроксид. Изтеглено от livestrong.com: livestrong.com.
- Формула на калциев хидроксид - Калциев хидроксид Използване, свойства, структура и формула. (2005-2017). Взето от softschools.com.
- Отравяне с калциев хидроксид. (2017, 7 февруари). Извлечено от medlineplus.gov.
- Химическа спецификация на калциев хидроксид. (S.F.). Взето от cameochemicals.noaa.gov.
- Готфрид Шмалц, Д. А. (2009). Биосъвместимост на денталните материали. Берлин: Спрингър.
- Информационен лист за безопасност Калциев хидроксид. (2013 г., 21 май). Изтеглено от sciencelab: sciencelab.com.
- Национален център за биотехнологична информация. (S.F.). PubChem Compound Database; CID = 6093208. Взето от pubchem.ncbi.nlm.nih.gov.
- Кралско химическо дружество. (2015). Калциев хидроксид. Извлечено от ChemSpider: chemspider.com.
- Russiver, M. (2015, 17 август). За какво се използва калциев хидроксид? Извлечено от quora: quora.com.


