Свойства на етил етер, структура, получаване, приложения
на етилов етер, известен също като диетилов етер, е органично съединение, чиято химична формула е С4Н10О. Той се характеризира с това, че е безцветна и летлива течност и следователно бутилките му трябва да се държат затворени възможно най-херметично..
Този етер е класифициран като член на диалкиловите етери; те имат формулата ROR ', където R и R' представляват различни въглеродни сегменти. И тъй като описва своето средно име, диетилов етер, са две радикали-етил тези, които се свързват с кислородния атом.

Първоначално етилов етер се използва като общ анестетик, въведен през 1846 г. от Уилям Томас Грийн Мортън. Въпреки това, поради неговата запалимост, неговата употреба е отхвърлена, заменяйки я с други по-малко опасни анестетици..
Това съединение се използва и за оценка на времето на кръвообращението по време на оценката на сърдечно-съдовия статус на пациентите.
В тялото диетиловият етер може да се трансформира в въглероден диоксид и метаболити; последният се отделя в урината. Обаче, по-голямата част от администрирания етер е издишан в белите дробове, без да претърпява никаква модификация.
От друга страна, той се използва като разтворител за сапуни, масла, парфюми, алкалоиди и смоли.
индекс
- 1 Структура на етилов етер
- 1.1 Междумолекулни сили
- 2 Физични и химични свойства
- 2.1 Други имена
- 2.2 Молекулна формула
- 2.3 Молекулно тегло
- 2.4 Физически вид
- 2.5 Миризма
- 2.6 Вкус
- 2.7 Точка на кипене
- 2.8 Точка на топене
- 2.9 Точка на запалване
- 2.10 Разтворимост във вода
- 2.11 Разтворимост в други течности
- 2.12 Плътност
- 2.13 Плътност на парите
- 2.14 Налягане на парите
- 2.15 Стабилност
- 2.16 Автоматично запалване
- 2.17 Разлагане
- 2.18 Вискозитет
- 2.19 Топлина на горене
- 2.20 Изпарителна топлина
- 2.21 Повърхностно напрежение
- 2.22 Йонизационен потенциал
- 2.23 Праг на мириса
- 2.24 Индекс на пречупване
- 3 Получаване
- 3.1 От етилов алкохол
- 3.2 От етилен
- 4 Токсичност
- 5 Използване
- 5.1 Органичен разтворител
- 5.2 Обща анестезия
- 5.3 Дух на етера
- 5.4 Оценка на кръвообращението
- 5.5 Обучителни лаборатории
- 6 Препратки
Структура на етилов етер
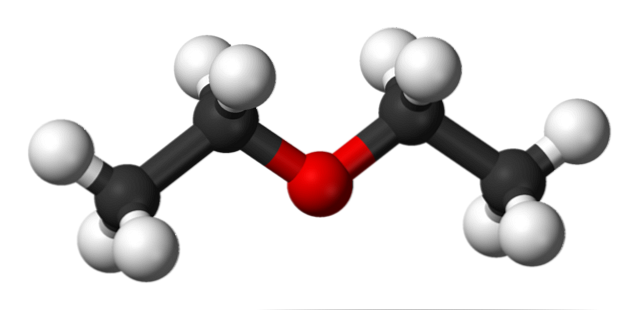
В изображението по-горе имаме представяне с модел на сфери и решетки на молекулната структура на етилов етер.
Както може да се види, червената сфера, съответстваща на кислородния атом, има две етилови групи, свързани с двете страни. Всички звена са прости, гъвкави и свободно въртящи се около осите σ.
Тези ротации създават стереоизомери, известни като конформери; че повече от изомерите, те са алтернативни пространствени състояния. Структурата на изображението съответства точно на анти-конформера, в който всичките му групи от атоми са разпределени (разделени една от друга).
Какъв ще бъде другият конформер? Затъмнените, и въпреки че изображението ви не е достъпно, просто ги визуализирате с U-образна форма.3, които биха изпитали стерилно отблъскване (те биха се сблъскали в пространството).
Затова се очаква, че молекулата на СН3СН2ОСН2СН3 приемете анти-конформацията през повечето време.
Междумолекулни сили
С какви интермолекулни сили молекулите на етиловия етер се управляват в течната фаза? Те се поддържат в течността главно благодарение на дисперсионните сили, тъй като в техния диполен момент (1.5D) липсва област с недостатъчна електронна плътност (δ +).
Това е така, защото никой въглероден атом на етилните групи не дава твърде много електронна плътност на кислородния атом. Горното е видно от картата на електростатичния потенциал на етиловия етер в ръка (дъното на изображението). Обърнете внимание на липсата на синя зона.
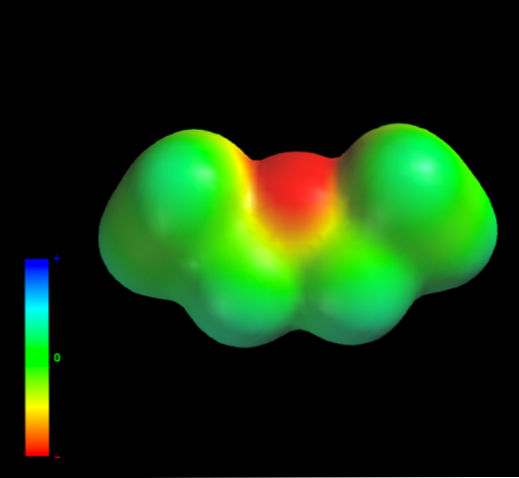
Кислородът също не може да образува водородни връзки, тъй като в молекулярната структура няма налични О-Н връзки. Следователно мигновените диполи и тяхната молекулна маса благоприятстват силите на разпръскване.
Въпреки това, той е силно разтворим във вода. Защо? Тъй като кислородният му атом, с по-висока електронна плътност, може да приеме водородни връзки от водната молекула:
(СН3СН2)2Оδ- - δ+Н-OH
Тези взаимодействия са отговорни за разтварянето на 6,04 g от този етер в 100 ml вода.
Физични и химични свойства
Други имена
-Диетилов етер
-етоксиетан
-Етил оксид
Молекулна формула
C4Н10О или (С2Н5)2О.
Молекулно тегло
74,14 g / mol.
Физически вид
Безцветна течност.
миризма
Сладки и пикантни.
вкус
Горещи и сладки.
Точка на кипене
94,3 ° F (34,6 ° С) до 760 mmHg.
Точка на топене
-177,3 ° F (-116,3 ° С). Стабилни кристали.
Точка на запалване
-49ºF (затворен контейнер).
Разтворимост във вода
6.04 g / 100 mL при 25 ° С.
Разтворимост в други течности
Смесва се с алифатни алкохоли с къса верига, бензол, хлороформ, петролев етер, мастен разтворител, много масла и концентрирана солна киселина.
Разтворим в ацетон и много разтворим в етанол. Също така е разтворим в нафта, бензен и масла.
плътност
0.714 mg / mL при 68 ° F (20 ° С).
Плътност на парите
2.55 (във връзка с въздуха, зает с плътност 1).
Парно налягане
442 mmHg при 68 ° F. 538 mmHg при 25 ° С. 58,6 kPa при 20 ° С.
стабилност
Бавно се окислява чрез въздействието на въздух, влага и светлина с образуването на пероксиди.
Образуването на пероксиди може да настъпи в етерни контейнери, които са били отворени и които остават на съхранение повече от шест месеца. Пероксидите могат да се детонират чрез триене, удар или нагряване.
Да се избягва контакт с: цинк, халогени, неметални оксихалиди, силни окислители, хромилхлорид, томентинови масла, нитрати и метални хлориди.
Автоматично запалване
356ºF (180ºC).
разлагане
Когато се затопли, той се разлага, излъчва остър и дразнещ дим.
вискозитет
0.2448 cPoise при 20 ° С.
Топлина на горене
8,807 Kcal / g.
Изпарителна топлина
89,8 cal / g при 30 ° С.
Повърхностно напрежение
17.06 дина / см при 20 ° С.
Йонизационен потенциал
9.53 eV.
Праг на мирис
0.83 ppm (чистотата не е дадена).
Индекс на пречупване
1,355 при 15 ° С.
получаване
От етилов алкохол
Етилов етер може да бъде получен от етилов алкохол, в присъствието на сярна киселина като катализатор. Сярната киселина във водна среда дисоциира, продуцирайки хидрониевия йон, Н3О+.
Безводният етилов алкохол преминава през разтвора на сярната киселина, нагрява се между 130 ° С и 140 ° С, като се получава протониране на молекули на етилов алкохол. Впоследствие друга молекула от непротониран етилов алкохол реагира с протонираната молекула.
Когато това се случи, нуклеофилната атака на втората молекула на етилов алкохол стимулира отделянето на вода от първата молекула (протонираната); в резултат на това се образува протониран етилов етер (СН3СН2OHCH2СН3), с частично зареден кислород.
Въпреки това, този метод на синтез губи ефективност, тъй като сярната киселина се разрежда с водата, получена в процеса (продукт на дехидратация на етилов алкохол)..
Температурата на реакцията е критична. При температури под 130 ° С реакцията е бавна и в по-голямата си част етиловият алкохол ще бъде дестилиран.
Над 150 ° С сярната киселина предизвиква образуването на етилен (двойната връзка алкен), вместо да се комбинира с етилов алкохол до образуване на етилов етер.
От етилен
В противоположния процес, т.е. хидратирането на етилена в парната фаза, етилов етер може да се образува като страничен продукт в допълнение към етилов алкохол. Всъщност, този синтетичен път произвежда по-голямата част от това органично съединение.
Този процес използва фосфорно-кисели катализатори, фиксирани към твърда подложка, като е в състояние да се регулира за получаване на повече етер.
Дехидратирането в парна фаза на етанол в присъствието на алумоокисни катализатори може да даде 95% добив при производството на етилов етер..
токсичност
Той може да предизвика дразнене на кожата и очите при контакт. Контактът с кожата може да причини изсушаване и напукване. Етерът обикновено не прониква през кожата, тъй като бързо се изпарява.
Дразненето на очите, причинено от етера, обикновено е слабо, а в случай на силно дразнене, увреждането обикновено е обратимо.
Поглъщането му предизвиква наркотични ефекти и дразнене на стомаха. Тежкото поглъщане може да причини увреждане на бъбреците.
Вдишването на етера може да предизвика дразнене на носа и гърлото. В случай на вдишване на етер може да настъпи сънливост, възбуда, замаяност, повръщане, нередовно дишане и повишено слюноотделяне..
Високата експозиция може да причини загуба на съзнание и дори смърт.
OSHA установява професионална граница на експозиция от 800 ppm средно по време на 8-часовата смяна.
Нива на дразнене на очите: 100 ppm (човек). Нива на дразнене на очите: 1200 mg / m3 (400 ppm).
приложения
Органичен разтворител
Това е органичен разтворител, който се използва за разтваряне на бром, йод и други халогени; по-голямата част от липидите (мазнините), смолите, чистите каучуци, някои алкалоиди, смоли, парфюми, целулозен ацетат, целулозен нитрат, въглеводороди и оцветители.
В допълнение, той се използва при извличането на активните съставки на животинските тъкани и растения, тъй като има по-ниска плътност от водата и плува върху него, оставяйки желаните вещества да се разтварят в етера..
Обща анестезия
Той се използва като общ анестетик от 1840 г., като замества хлороформа за терапевтично предимство. Въпреки това, той е запалимо вещество и следователно среща сериозни трудности при използването му в клинични условия.
В допълнение, той произвежда при пациенти някои нежелани постоперативни странични ефекти като гадене и повръщане.
Поради тези причини използването на етер като обща анестезия е изхвърлено, замествайки го с други анестетици като халотан..
Дух на етера
Етерът, смесен с етанол, се използва за образуване на разтвора, наречен спирт на етер, използван за лечение на гастричен мехур и леки форми на гастралгия.
Оценка на кръвообращението
Етерът е използван за оценка на кръвообращението между ръката и белите дробове. Етерът се инжектира в ръка, привеждайки кръвта в дясното предсърдие, след това в дясната камера и оттам в белите дробове..
Времето, което изтича от инжектирането на етера, до поемането на етерния мирис в издишания въздух, е приблизително 4 до 6 s..
Обучителни лаборатории
Етерът се използва в учебните лаборатории при много експерименти; например в демонстрацията на законите на Мендел за генетика.
Етерът се използва, за да отслаби мухите от рода Drosophila и да позволи необходимите пресичания между тях, за да се докажат законите на генетиката
препратки
- Греъм Соломонс T.W., Крейг Б. Фрайле. (2011 г.). Органична химия. Амини. (10тата издание.). Wiley Plus.
- Кери Ф. (2008). Органична химия (Шесто издание). Mc Graw Hill.
- Sevier. (2018). Диетилов етер. Science Direct. Възстановен от: sciencedirect.com
- Редакторите на Encyclopaedia Britannica. (2018). Етилов етер. Britannica ncyclopædia. Изтеглено от: britannica.com
- PubChem (2018). Етер. Възстановен от: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Диетилов етер. Изтеглено от: en.wikipedia.org
- Лист за безопасност XI: етилов етер. [PDF]. Възстановен от: quimica.unam.mx


